Aminohapped ja valgud on mineraalmaailmast elusolendisse liikumise vaheühendid.
Nagu nimigi ütleb, on aminohapped bifunktsionaalsed orgaanilised ained: koosnevad aminofunktsioonist (-NH2) ja karboksüülfunktsioonist (-COOH); need võivad olla α, β, γ jne, sõltuvalt aminorühma asendist karboksürühma suhtes:



Bioloogiliselt olulised aminohapped on kõik α-aminohapped.
Valgu struktuurid koosnevad kahekümnest aminohappest.
Nagu ülaltoodud üldistest struktuuridest näha, on kõigil aminohapetel ühine osa ja erinev osa, mis neid iseloomustab (tähistatakse üldjoontes R -ga).
Kahekümnest aminohappest üheksateist on optiliselt aktiivsed (need suunavad polariseeritud valguse tasapinna kõrvale).
Enamikul aminohapetel on ainult üks aminorühm ja üks karboksüülrühm, seetõttu nimetatakse neid neutraalsed aminohapped; neid, millel on lisakarboksüül, nimetatakse happelised aminohapped samas kui need, kellel on täiendav aminorühm, on aluselised aminohapped.
Aminohapped on kristallilised tahked ained ja neil on hea vees lahustuvus.
Mõnede aminohapete puudumine toidus põhjustab tõsiseid muutusi arengus; tegelikult ei suuda inimorganism sünteesida mõningaid aminohappeid, mida nimetatakse täpselt asendamatuteks (need tuleb sisse viia koos toiduga), samas kui ta suudab ise toota ainult mõningaid aminohappeid (mitteolemuslikke).
Üks haigusi, mis on tingitud asendamatute aminohapete puudumisest, on haigus, mida tuntakse nimega kwashiorkor (sõna, mis pärineb Aafrika murdest, mis tõlkes tähendab "esimene ja teine"); see haigus mõjutab esmasündinuid, kuid pärast teise lapse sündi, sest esimesel lapsel puudub ema piim, mis sisaldab õiget valguvaru. Seetõttu on see haigus alatoidetud elanikkonna seas laialt levinud ja sellega kaasneb kõhulahtisus, isutus, mis viib organismi järkjärgulise nõrgenemiseni.
Nagu juba mainitud, on looduslikel aminohapetel, välja arvatud glütsiin (see on R-rühma asemel vesinikuaatom ja see on kahekümnest väikseim), vähemalt ühe asümmeetrilise olemasolu tõttu optiline aktiivsus süsinik. Looduslikes aminohapetes kuulub L -seeriasse asümmeetrilise süsiniku absoluutne konfiguratsioon, millega on seotud ainult amino- ja karboksürühm;
D-aminohapped ei muutu kunagi valgu struktuuri osaks.
Me mäletame seda:
DNA ---- transkriptsioon → m-RNA ---- translatsioon → valk
Transkriptsioon on võimeline kodeerima L-aminohapetena; D-aminohappeid võib sisaldada mitte-valgulistes struktuurides (nt bakterite vooderdiseinas: bakterites puudub "geneetiline teave D-aminohapete kaitsmiseks", ent ensüümide kohta on olemas "geneetiline teave" mis tegelevad bakterite vooderdiseinaga).
Tuleme tagasi aminohapete juurde: R -rühma erinev struktuur määrab iga aminohappe individuaalsed omadused ja annab konkreetse panuse valkude omadustesse.
Seetõttu arvati aminohapete jagamist R -rühma olemuse alusel:
Polaarsed, kuid laenguta aminohapped:
Glütsiin (R = H-)
Seriin (R = HO-CH2-)
Treoniinhädavajalik
Treoniinil on kaks sümmeetriakeskust: looduses eksisteerib ainult 2S, 3R treoniin.
Treoniin on asendamatu aminohape (mitte segi ajada asendamatutega: kõik aminohapped on asendamatud), seega tuleb seda võtta koos toiduga, st seda sisaldavate toitude söömisega, sest nagu juba mainitud, geneetilist pärandit ei esine Inimese rakud suudavad seda aminohapet toota (seda pärandit leidub paljudes taimedes ja paremates).
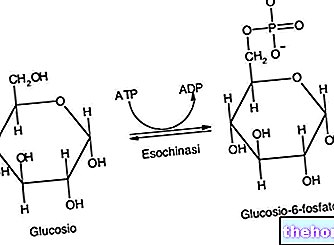
Seriini ja treoniini hüdroksüülrühma saab esterdada fosforüülrühmaga (saades fosfoseriini ja fosfotreoniini), seda protsessi nimetatakse fosforüülimine; fosforüülimist kasutatakse looduses signaalide teisendamiseks raku sees ja väljas.
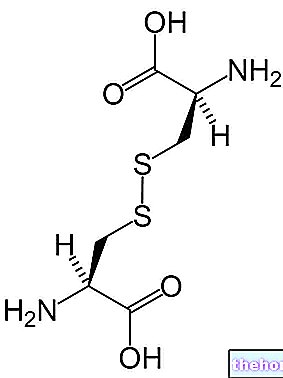
Tsüsteiin (R = HS-CH2-)
Tsüsteiini sulfhüdrüülrühm on kergemini protoneeritav kui seriini hüdroksüülrühm: väävel ja hapnik kuuluvad mõlemad kuuendasse rühma, kuid väävel on kergemini oksüdeeritav, kuna sellel on suuremad mõõtmed.
Türosiin [R = HO- (C6H4) -CH2-]
N.B.
(C6H4) = di-asendatud benseenitsükkel
Nagu seriini ja treoniini puhul, saab hüdroksüüli esterdada (fosforüülida).Asparagiin (R = NH2-CO-CH2-)
Glutamiin (R = NH2-CO-CH2-CH2-)
Mittepolaarsed aminohapped
neil on hüdrofoobsed külgrühmad; Selles klassis eristame:
Alifaatikumid:
Alaniin (R = CH3-)
Valiin (R = (CH3) 2-CH-) oluline
Leutsiin (R = (CH3) 2-CH-CH2-) hädavajalik
Isoleutsiin (R =
) hädavajalik
Metioniin (R = CH3-S-CH2-CH2-) hädavajalik
Rakumembraanid koosnevad kahekordsest lipiidkihist, mille valgud on ankurdatud tänu nende hüdrofoobsele iseloomule, seetõttu sisaldavad need alaniini, valiini, isoleutsiini ja leutsiini. Metioniin seevastu on aminohape, mida esineb peaaegu alati väikestes kogustes (umbes 1%).
Proline
Aromaatne:
Fenüülalaniin (R = Ph-CH2-) Ph = fenüül: oluline monoasendatud benseen
Trüptofaan (R =
hädavajalik
Need kaks aminohapet, olles aromaatsed, neelavad ultraviolettkiirguse läheduses (umbes 300 nm); seetõttu on võimalik kasutada neid UV -spektrofotomeetria meetodeid, et määrata neid aminohappeid sisaldava teadaoleva valgu kontsentratsioon.
Laetud aminohapped
Need jagunevad omakorda:
Happelised aminohapped (millel on polaarsed jäägid negatiivse laenguga pH 7 juures) on sellised, kuna nad suudavad anda positiivse H + laengu:
Asparagiinhape
Glutamiinhape (R =
)
Need aminohapped pärinevad vastavalt asparagiinist ja glutamiinist; kõik neli eksisteerivad looduses ja see tähendab, et c "on igaühe jaoks spetsiifiline teave, see tähendab c" on baastrepp DNA -s, mis kodeerib neid kõiki.
Põhilised aminohapped (millel on polaarsed jäägid positiivse laenguga pH 7 juures) on sellised, kuna nad suudavad vastu võtta positiivse H + laengu:
Lüsiin (R =
) hädavajalik
Arginiin (R =
)
Histidiin (R =
)
On valke, mille kõrvalahelates on aminohapete derivaate: näiteks võib esineda fosfoseriini (puudub geneetiline teave, mis kodeerib fosfoseriini, ainult seriini); fosfoseriin on modifikatsioon tõlkimisjärgne: pärast valkude sünteesi
DNA ---- transkriptsioon → m-RNA ---- translatsioon → valk
sellised translatsioonijärgsed modifikatsioonid võivad esineda valgu külgahelates.
Vaata ka: Valgud, pilk keemiale


















-cause-e-rimedi.jpg)