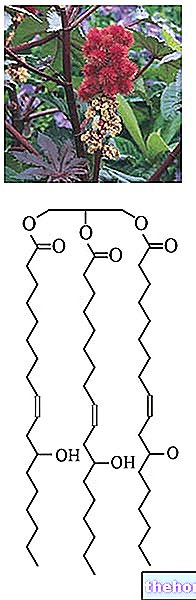
Looduses leidub magneesiumi kõrge reaktiivsuse tõttu ühendite ja magneesiumisoolade kujul.
Kui me jälgime selle keemilise elemendi elektroonilist konfiguratsiooni, märkame tegelikult kahe elektroni olemasolu äärepoolseimal orbitaalil; need elektronid kantakse kerge vaevaga üle teistele keemilistele elementidele, mis vajavad välise energiataseme lõpuleviimiseks elektrone; kahest magneesiumist ilma elektronid on positiivselt laetud → magneesiumioon Mg ++; kui selle asemel jälgime kloori elektroonilist konfiguratsiooni, märkame seitsme elektroni olemasolu välisel orbitaalil; seetõttu kipub kloor okteti täiendamiseks ahnelt enda juurde meelitama elektroni; sel viisil, kui puuduv elektron on omandatud, kannab see klooriiooni nime Cl-. Siin selgitatakse, kuidas moodustub magneesiumkloriid (Mg Cl2).

Pärast seda lühikest keemilist kõrvalekaldumist vaatame lühidalt erinevate ühendite ja magneesiumisoolade terviseomadusi.
Esimene omadus, mida magneesiumiühendi hindamisel tervise seisukohast arvesse võtta, on selles sisalduva elementaarse magneesiumi kogus; eespool kirjeldatud juhul on ilmne, et üks gramm magneesiumkloriidi sisaldab teatud protsenti elementaarset kloori ja teatud kogust elementaarset magneesiumi.
Teades, kui palju elementaarset magneesiumi on erinevates ühendites ja soolades, saame teada toote kogust, mida tuleb selle mineraali igapäevase vajaduse katmiseks võtta.
(aastat)
(mg / päevas)
(mg / päevas)
(mg / päevas)
(mg / päevas)
Kuna ühendeid ja magneesiumisoolasid kasutatakse sageli selle mineraali taseme tõstmiseks kehas ja puuduste kõrvaldamiseks, tundub loogiline liikuda suurema elementaarse magneesiumisisaldusega ühendite ja soolade tarbimise poole. Tegelikult on see aspekt allutatud inimese soolestiku võimekus neelata ühendis sisalduvat magneesiumi (vt põhjalik analüüs). Sel põhjusel on spetsiifiliste magneesiumipuuduste täitmiseks oluline valida parimad imenduvad allikad, samas kui muude rakenduste puhul - näiteks antatsiidne või lahtistav toime - eelistatakse ühendeid, mis inimese soolestikus oluliselt ei imendu.
Üldiselt on kõige paremini imenduvad magneesiumisoolad need, milles mineraal on seotud orgaaniliste ühenditega (glükonaat, aspartaat, püruvaat, malaat, tsitraat, pidolaat, laktaat või orotaat). Kuid isegi magneesiumkloriid on hästi imenduv allikas ning eelistega võrreldes on selle eeliseks madal hind. Seevastu teised anorgaanilise magneesiumi allikad (magneesiumoksiid, magneesiumkarbonaat, magneesiumsulfaat) on neis sisalduva magneesiumi biosaadavuse osas suure kriitika objektiks. Kahjuks ei ole sellel teemal avaldatud teaduslikest uuringutest siiski piisav, et kindlalt kindlaks teha erinevate magneesiumiühendite rakendusi tervisele, arvestades väheste uuringute olemasolu, mille tulemused on sageli vastuolulised. Sel põhjusel tuleb järgnevat - teadusartiklite ja ülikoolitekstide uuesti lugemise tulemust - käsitleda piisavalt ettevaatlikult.
Seda peetakse hästi imenduvaks magneesiumisoolaks; näiteks ühes uuringus on näidatud, et see imendub 4,5 korda paremini kui anorgaaniline ühend magneesiumoksiid; tsitraadi olemasolu võib olla kasulik juhul, kui on vaja tõsta uriin, näiteks kalduvuse korral kusihappele ja / või tsüstiinkividele
See on tuntud eelkõige uuringu kohta, mis tõestas selle võimalikku efektiivsust premenstruaalse sündroomi ravis.Püruglaamhappe olemasolu näib andvat sellele soolale neuroseerivat toimet.
Orgaaniline sool, mille seedimistasandil on parem talutavus ja imenduvus võrreldav teiste orgaaniliste vormidega; Toiduohutust hindav Euroopa ametiasutus EFSA on väljendanud muret ohu pärast, et orohape soodustab erinevate teadaolevate kantserogeenide poolt põhjustatud kasvajate teket
Vees hästi lahustuv, tundub, et sellel on suurepärane imenduvus
Sellel magneesiumiallikal on kõigist anorgaanilistest vormidest parim vees lahustuvus. Järelikult, nagu on näidanud erinevad uuringud, on selle biosaadavus sarnane või igal juhul veidi madalam kui kõige kuulsamatel orgaanilistel sooladel, mille eeliseks on madalam hind. Turul leidub spetsiifiliste mineraalsete toidulisandite puhul magneesiumkloriidi ka kaetud tablettide kujul, et parandada mao talutavust.
Kuigi see on elementaarse magneesiumi rikkaim ühend, tekitab see kõige suuremat kriitikat organismi imendumise võimalikkuse suhtes. Vees halvasti lahustuv, on see mitmetes uuringutes näidanud halba biosaadavust võrreldes teiste magneesiumivormidega. eeldatakse, et vees paremini lahustuvad peened valmistised imenduvad paremini kui need, millel on jämedam tera.
Seda kasutatakse antatsiidi ja lahtistina: see on näiteks üks kahest Maaloxi toimeainest. Arvestades vähest lahustuvust vees, omistatakse sellele üldiselt madal biosaadavus, kuigi ühes uuringus tõestati, et see suurendab magneesiumi taset uriinis võrreldaval määral mõne orgaanilise soolaga, näiteks magneesiumtsitraadiga.
Vees väga lahustuv ja inimkeha halvasti imenduv, seda EI kasutata tavaliselt magneesiumi allikana toidulisandites ega rikastatud toitudes. Pigem kasutatakse seda tavaliselt antatsiidina
Seda kasutatakse haiglates magneesiumi intramuskulaarseks või intravenoosseks manustamiseks. Seda kasutatakse ka lahtistina suurtes annustes (20 g), sageli inglise soola või Epsomi sool. Selles soolas sisalduva magneesiumi biosaadavust suukaudsel manustamisel peetakse madalaks