Et saaksime arusaadavalt rääkida "hemoglobiin (Hb), on kasulik hoolitseda esimese eest müoglobiin (Mb) mis on väga sarnane hemoglobiiniga, kuid on palju lihtsam. Hemoglobiini ja müoglobiini vahel on tihedad sugulussuhted: mõlemad on konjugeeritud valgud ja nende proteesirühm (mittevalguline osa) on rühm heme.
Müoglobiin on kerajas valk, mis koosneb ühest viiekümne aminohappe ahelast (see sõltub organismist) ja selle molekulmass on umbes 18 Kd.
Nagu mainitud, on see varustatud heemirühmaga, mis on sisestatud valgu hüdrofoobsesse (või lipofiilsesse) ossa, mis koosneb kiudvalkude a-heeliksstruktuuridele omastest voltidest.
Müoglobiin koosneb peamiselt a-heeliksite segmentidest, mida esineb kaheksa ja koosneb peaaegu eranditult mittepolaarsetest jääkidest (leutsiin, valiin, metioniin ja fenüülalaniin), polaarseid jääke aga praktiliselt ei esine (asparagiinhape, glutamiinhape, lüsiin) ja arginiin); ainsad polaarsed jäägid on kaks histidiini, millel on põhiline roll hapniku sidumisel heemirühmaga.
Hemirühm on kromofoorrühm (imendub nähtavasse) ja on müoglobiini funktsionaalne rühm.
Vaata ka: glükeeritud hemoglobiin - hemoglobiin uriinis
Natuke keemiast

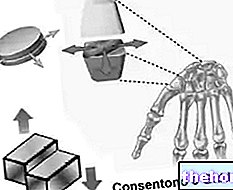
Protoporfüriini ja raua vaheline side on tüüpiline koordineerivate ühendite side, mis on keemilised ühendid, milles keskne aatom (või ioon) moodustab sidemeid teiste keemiliste liikidega, mille arv on suurem kui selle oksüdatsiooniarv (elektrilaeng). Hemi puhul on need sidemed pöörduvad ja nõrgad.
Raua koordineerimisnumber (koordinatsioonisidemete arv) on kuus: raua ümber võib olla kuus molekuli, mis jagavad siduvaid elektrone.
Koordineerimisühendi moodustamiseks kulub kaks korrektselt orienteeritud orbitaali: üks suudab "omandada" elektrone ja teine neid annetada.
Hemis moodustab raud neli tasapinnalist sidet, mille proto-porfüriinitsükli keskel on neli lämmastikuaatomit ja viies side proksimaalse histidiinlämmastikuga; raual on kuues vaba koordineeriv side ja see võib seostuda hapnikuga.
Kui raud on vaba iooni kujul, orbiiditakse selle tüüp d neil kõigil on sama energia; müoglobiinis on raudioon seotud protoporfüriini ja histidiiniga: need liigid häirivad orbitaale magnetiliselt d natuke rauda; häirete ulatus on erinevate orbitaalide puhul erinev d sõltuvalt nende ruumilisest orientatsioonist ja häirivatest liikidest. Kuna orbitaalide koguenergia peab olema konstantne, põhjustab häirimine erinevate orbitaalide vahel energeetilist eraldumist: mõne orbitaali omandatud energia on samaväärne teiste kaotatud energiaga.
Kui orbitaalide vaheline eraldatus ei ole väga suur, on eelistatav kõrge spinniga elektrooniline paigutus: siduvad elektronid püüavad end paigutada paralleelsete keerutustega võimalikult paljudele alamtasanditele (maksimaalne paljusus); kui aga häirimine on väga tugev ja orbitaalide vahel on suur vahe, võib olla mugavam sidemeelektronide sidumine madalama energiaga (madala keerutusega) orbitaalidel.
Kui raud seostub hapnikuga, eeldab molekul madalat tsentrifuugimist, samas kui raua kuues koordinatsiooniside on vaba, on molekulil kõrge tsentrifuugimissüsteem.
Tänu sellele tsentrifuugimise erinevusele saame müoglobiini spektraalanalüüsi abil mõista, kas hapnik (MbO2) on sellega seotud või mitte (Mb).
Müoglobiin on tüüpiline lihasvalk (kuid seda ei leidu ainult lihastes).
Müoglobiin ekstraheeritakse kašelotist, milles seda on suures koguses, ja seejärel puhastatakse.
Vaalalastel on hingamine nagu inimestel: kopsudega peavad nad hingamisprotsessi kaudu õhku imama; kašelott peab viima võimalikult palju hapnikku lihastesse, mis suudavad koguneda hapnikku, sidudes selle neis sisalduva müoglobiiniga; seejärel vabaneb hapnik vaalalise kastmisel aeglaselt, sest tema ainevahetus nõuab hapnikku: seda suurem on kogus hapnikku, mida kašelott suudab absorbeerida ja mida rohkem sukeldumise ajal hapnikku on.
Müoglübiin seob hapniku pöörduvalt ja seda esineb perifeersetes kudedes suuremal protsendil, seda enam, et kude on harjunud töötama ajas kaugete hapnikuvarudega.
<--- Müoglobiin on lihastes esinev valk, mille ülesanne on täpselt hapniku "reservuaar".
Enam -vähem punaseks teeb liha hemoproteiinide sisaldus (just heem muudab liha punaseks).
Hemoglobiinil on palju struktuurilisi sarnasusi müoglobiiniga ja see on võimeline siduma molekulaarset hapnikku pöörduvalt; kuid kuigi müoglobiin piirdub lihaste ja perifeersete kudedega üldiselt, leidub hemoglobiini erütrotsüütides või punastes verelibledes (need on pseudorakud, st nad ei ole pärisrakud), mis moodustavad 40% verest.
Vastupidiselt müoglobiinile on hemoglobiini töö hapniku võtmine kopsudesse, selle vabastamine rakkudesse, kus seda vajatakse, süsinikdioksiidi võtmine ja kopsudesse vabastamine, kus tsükkel algab uuesti.
L "hemoglobiin see on tetrameeter, see tähendab, et see koosneb neljast polüpeptiidahelast, millest igaühel on heemrühm ja mis on identsed kahe kaupa (inimesel on kaks alfa- ja kaks beetahelat).
Hemoglobiini põhiülesanne on hapniku transport; teine vere funktsioon, milles hemoglobiin osaleb, on ainete transport kudedesse.
Teel kopsudest (palju hapnikku) kudedesse kannab hemoglobiin hapnikku (samal ajal jõuavad teised ained kudedesse), vastupidisel teel aga kudede kogutud jäätmeid, eriti süsinikku ainevahetuses tekkiv dioksiid.
Inimese arengus on geene, mida ekspresseeritakse ainult teatud aja jooksul; sel põhjusel on erinevad hemoglobiinid: täiskasvanud mehe loote-, embrüonaalsed.
Ahelad, millest need erinevad hemoglobiinid koosnevad, on erineva struktuuriga, kuid mõningate sarnasustega on nende ülesanne tegelikult enam -vähem sama.
Mitme erineva ahela olemasolu selgitus on järgmine: organismide evolutsiooniprotsessi käigus on arenenud isegi hemoglobiin, mis on spetsialiseerunud hapniku transportimisele selle rikastest piirkondadest puudulikesse piirkondadesse. "Alguses evolutsiooniahela l "hemoglobiin kandis väikestes organismides hapnikku; evolutsiooni käigus jõudsid organismid suurematesse mõõtmetesse, seetõttu muudeti hemoglobiini nii, et see oleks võimeline transportima hapnikku kaugematesse piirkondadesse, kus see oli rikas; seda tehes on nad evolutsiooniprotsessi käigus kodeerinud uued ahelate struktuurid, mis moodustavad hemoglobiini.
Müoglobiin seob hapnikku isegi mõõduka rõhu korral; perifeersetes kudedes on rõhk (PO2) umbes 30 mmHg: müoglobiin ei vabasta sellel rõhul hapnikku, seega oleks see hapniku kandjana ebaefektiivne. Hemoglobiin seevastu , sellel on elastsem käitumine: see seob hapniku kõrge rõhuga ja vabastab selle, kui rõhk väheneb.
Kui valk on funktsionaalselt aktiivne, võib see oma kuju veidi muuta; näiteks hapnikuga rikastatud müoglobiin on erineva kujuga kui hapnikuga rikastamata müoglobiin ja see mutatsioon ei mõjuta selle naabreid.
Seotud valkude, näiteks hemoglobiini puhul on olukord teistsugune: kui ahel hapnikuga rikastatakse, kutsutakse see oma kuju muutma, kuid see modifikatsioon on kolmemõõtmeline, mistõttu mõjutatakse ka teisi tetrameetri ahelaid. soovitab, et ühe modifitseerimine mõjutaks teisi naabreid isegi erineval määral; kui ahel hapnikuga rikastab, võtavad teised tetrameetri ahelad hapniku suhtes "vähem vaenuliku hoiaku": selle ahela raskus hapnikusisaldus väheneb, kuna selle lähedased ahelad hapnikutavad omakorda. Sama kehtib ka deoksügeenimise kohta.
Deoksühemoglobiini kvaternaarset struktuuri nimetatakse T (pingeline) vormiks, samas kui oksühemoglobiini oma nimetatakse R (vabanenud) vormiks; pingelises olekus on happeliste aminohapete ja aluseliste aminohapete vahel üsna tugev elektrostaatiline koostoime, mille tulemuseks on deoksühemoglobiini jäik struktuur (see on põhjus, miks "pingeline vorm"), samas kui hapnikuga ühendamisel on nende olemus interaktsioonid vähenevad (seega "vabastatud vorm"). Veelgi enam, hapniku puudumisel stabiliseerub histidiini laeng (vt struktuur) asparagiinhappe vastupidise laenguga, samas kui hapniku juuresolekul on valgu kalduvus kaotada prooton; kõik see tähendab, et hapnikuga rikastatud hemoglobiin on tugevam hape kui deoksügeenitud hemoglobiin: bohri efekt.
Sõltuvalt pH -st seondub heemirühm enam -vähem kergesti hapnikuga: happelises keskkonnas vabastab hemoglobiin kergemini hapnikku (pingeline vorm on stabiilne), samas kui aluselises keskkonnas on side hapnikuga raskem.

Iga hemoglobiin vabastab 0,7 prootonit siseneva hapniku (O2) mooli kohta.
Bohri efekt võimaldab hemoglobiinil parandada hapniku kandmise võimet.
Hemoglobiin, mis liigub kopsudest kudedesse, peab tasakaalustama rõhu, pH ja temperatuuri funktsioonina.
Vaatame temperatuuri mõju.
Temperatuur kopsu alveoolides on umbes 1-1,5 ° C madalam kui välistemperatuur, samas kui lihastes on temperatuur umbes 36,5-37 ° C; temperatuuri tõustes küllastustegur langeb (samal rõhul): see juhtub, sest kineetiline energia suureneb ja dissotsiatsioon on soositud.

On ka teisi tegureid, mis võivad mõjutada hemoglobiini võimet hapnikuga seonduda, millest üks on 2,3 bisfosfoglütseraadi kontsentratsioon.
2,3 bisfosfoglütseraat on erütrotsüütides esinev metaboolne aine kontsentratsioonis 4-5 mM (üheski teises organismi osas ei esine seda nii kõrge kontsentratsiooniga).
Füsioloogilise pH juures deprotoneeritakse 2,3 bisfosfoglütseraat ja sellel on viis negatiivset laengut; see on kiilutud kahe hemoglobiini beetahela vahele, kuna neil ahelatel on suur positiivsete laengute kontsentratsioon. Beetahelate ja 2,3 -bisfosfoglütseraadi elektrostaatiline koostoime annab süsteemile teatud jäikuse: saadakse pingeline struktuur, millel on väike afiinsus hapniku suhtes; hapnikuga varustamise ajal väljutatakse 2,3 -bisfosfoglütseraat.
Erütrotsüütides on c "spetsiaalne aparaat, mis muundab 1,3-bisfosfoglütseraadi (toodetud ainevahetuse teel) 2,3-bisfosfoglütseraadiks nii, et selle kontsentratsioon jõuab 4-5 mM ja seetõttu on hemoglobiin võimeline kudedes hapnikku vahetama.
Koesse saabuv hemoglobiin on vabanenud olekus (seotud hapnikuga), kuid koe läheduses on see karboksüleeritud ja läheb pingesse olekusse: sellises olekus oleval valgul on vähem kalduvust hapnikuga seonduda. vabanenud olekusse, seetõttu vabastab hemoglobiin kudedesse hapniku; pealegi tekib vee ja süsinikdioksiidi reaktsioonil H + ioonide, seega bohri efekti tõttu hapnikku.
Süsinikdioksiid difundeerub plasmamembraani läbivasse erütrotsüütidesse; Kuna erütrotsüüdid moodustavad umbes 40% verest, peaksime eeldama, et ainult 40% kudedest hajuvast süsinikdioksiidist siseneb nendesse, tegelikult 90% süsinikdioksiidist siseneb erütrotsüütidesse, kuna need sisaldavad ensüümi, mis muundab süsinikdioksiidi süsinikhappes annab see tulemuseks, et süsinikdioksiidi statsionaarne kontsentratsioon erütrotsüütides on madal ja seetõttu on sisenemiskiirus kõrge.

Teine nähtus, mis ilmneb, kui erütrotsüüt jõuab koesse, on järgmine: gradiendi järgi väljub "HCO3- (süsinikdioksiidi derivaat)" erütrotsüüdist ja negatiivse laengu väljundi tasakaalustamiseks siseneme "kloriididesse, mis määrab osmootse rõhu tõusu: selle variatsiooni tasakaalustamiseks toimub ka vee sisenemine, mis põhjustab erütrotsüütide turset (HAMBURGERi efekt). Vastupidine nähtus ilmneb siis, kui erütrotsüüt jõuab kopsu alveoolidesse: erütrotsüütide deflatsioon (HALDANE efekt) Seetõttu on venoossed erütrotsüüdid (suunatud kopsudesse) ümaramad kui arteriaalsed.