Et rääkida kahekümnest aminohappest, mis moodustavad valgu struktuurid ja modifitseeritud, oleks vaja kirjeldada vähemalt kaksteist spetsialiseerunud ainevahetusrada.
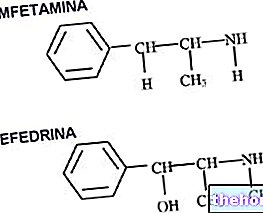
Kuid miks kasutavad rakud aminohapete kataboliseerimiseks nii palju ainevahetusradasid, mis nõuavad energiat (näiteks ensüümide katalüütiliste saitide taastamiseks), millest igaühel on ensümaatiline pärimus? Peaaegu kõigist aminohapetest on võimalik spetsiaalsete radade kaudu saada metaboliite, mida kasutatakse vähesel määral energia tootmiseks (näiteks glükoneogeneesi ja ketoonkehade raja kaudu), kuid mis viivad eelkõige komplekside moodustumiseni. molekulid, milles on palju süsinikuaatomeid (näiteks fenüülalaniinist ja türosiinist, hormoone toodetakse selleks otstarbeks neerupealistes); kui ühelt poolt oleks lihtne toota energiat aminohapetest, siis teisest küljest oleks keeruline keerukate molekulide ehitamine väikestest molekulidest lähtudes: aminohapete katabolism võimaldab neil oma luustikku kasutada suuremate liikide saamiseks.
Tervislik inimene lagundab iga päev kaks või kolm hektogrammi aminohappeid: 60–100 g neist pärineb toiduga kaasnevatest valkudest, kuid üle 2 hektogrammi saadakse organismi lahutamatuks osaks olevate valkude normaalsest käibest ( nende valkude aminohapped, mida redoksprotsessid kahjustavad, asendatakse teistega ja kataboliseeritakse).
Aminohapped annavad ATP-s energiat: pärast α-aminorühma eemaldamist võivad järelejäänud aminohapete skeletid pärast sobivaid muundamisi siseneda krebsi tsüklisse. Lisaks, kui toitainete pakkumine on puudulik ja glükoosi kogus väheneb, aktiveerub glükoneogenees: glükoneogeneetilised aminohapped on need, mida pärast sobivaid muudatusi saab glükoneogeneesi viia; glükoneogeneetilised aminohapped on need, mida saab muundada püruvaat või fumaraat (fumaraadi saab muundada malaadiks, mis lahkub mitokondrist ja tsütoplasmas muundatakse oksaloatsetaadiks, millest saab fosfoenoolpüruvaati). äädikas-atsetaat.
Äsjakirjeldatu on väga oluline aspekt, sest aminohapped võivad suhkruvaeguse kohese paastumise korral parandada; kui paastumine kestab, sekkub kahe päeva pärast lipiidide ainevahetus (kuna valgu struktuure ei saa liiga palju rünnata), kuna selles glükoneogenees on väga piiratud, muundatakse rasvhapped atsetüülkoensüüm A ja ketoonkehadeks. Alates edasisest paastumisest kohaneb aju ka ketoonkehade kasutamisega.
Α-aminorühma ülekanne aminohapetest toimub transaminatsioonireaktsiooni kaudu; ensüümid, mis seda reaktsiooni katalüüsivad, ütlevad nad tegelikult, transaminaasid (või aminotransferaas). Need ensüümid kasutavad ensümaatilist kofaktorit nimega püridoksaalfosfaat, mis sekkub oma aldehüüdrühmaga. Püridoksaalfosfaat on püridoksiini fosforüülimise produkt, mis on peamiselt köögiviljades leiduv vitamiin (B6).
Transaminaasidel on järgmised omadused:
Kõrge spetsiifilisus a-ketoglutaraadi-glutamaadi paarile;
Nad on nime saanud teise paari järgi.
Transaminaasi ensüümid hõlmavad alati a-ketoglutaraadi-glutamaadi paari ja neid eristatakse teise kaasatud paari järgi.
Näited:
L "aspartaadi transaminaas st GOT (glutamaat-ossalatsetaat-transaminaas): ensüüm kannab a-aminorühma aspartaadilt üle a-ketoglutaraadile, saades oksaloatsetaadi ja glutamaadi.
L "alaniini transaminaas st GTP (glutamaat-püruvaadi transaminaas): ensüüm kannab a-aminorühma "alaniinilt" a-ketoglutaraadile, saades püruvaadi ja glutamaadi.
Erinevad transaminaasid kasutavad α-ketogluraati aminohapete aminorühma aktsepteerijana ja muudavad selle glutamaadiks; samas kui moodustunud aminohappeid kasutatakse ketoonkehade rajal.
Seda tüüpi reaktsioonid võivad toimuda mõlemas suunas, kuna need purunevad ja moodustavad sama energiasisaldusega sidemed.
Transaminaasid asuvad nii tsütoplasmas kui ka mitokondris (need on enamasti tsütoplasmas aktiivsed) ja erinevad oma isoelektrilise punkti poolest.
Transaminaasid on võimelised ka aminohappeid dekarboksüülima.
Peab olema võimalus muuta glutamaat tagasi α-ketoglutaraadiks: seda tehakse deaminatsiooni teel.
Seal glutamaatdehüdrogenaas see on ensüüm, mis on võimeline muundama glutamaadi a-ketoglutaraadiks ja seega muutma glutamaadi kujul leiduvate aminohapete aminorühmad ammoniaagiks. Toimub redoksprotsess, mis läbib vahe-α-aminoglutaraadi: ammoniaak ja a-ketoglutaraat vabanevad ja naasevad ringlusse.
Seejärel läbib aminohapete aminorühmade kõrvaldamine transaminaasid (mis erinevad substraadi järgi) ja glutamaatdehüdrogenaasi, mis määrab ammoniaagi moodustumise.
Glutamaatdehüdrogenaasi on kahte tüüpi: tsütoplasmaatiline ja mitokondriaalne; kofaktor, mis on ka selle ensüümi kosubstraat, on NAD (P) +: glutamaatdehüdrogenaas kasutab vähendava jõu vastuvõtjana kas NAD + või NADP +. Tsütoplasmaatiline vorm eelistab, kuigi mitte ainult, NADP +, samas kui mitokondriaalne vorm eelistab NAD +. Mitokondriaalse vormi eesmärk on aminorühmade kõrvaldamine: see viib ammoniaagi (mis on mitokondrite spetsialiseeritud ensüümi substraat) ja NADH (mis saadetakse hingamisahelasse) moodustumiseni. Tsütoplasmaatiline vorm töötab vastupidises suunas, see tähendab, et ta kasutab ammoniaaki ja a-ketoglutaraati glutamaadi (mille biosünteetiline sihtkoht) saamiseks: see reaktsioon on redutseeriv biosüntees ja kasutatud kofaktor on NADPH.
Glutamaatdehüdrogenaas toimib siis, kui on vaja kõrvaldada aminohapete aminorühmad, näiteks ammoniaak (uriini kaudu), või kui energia tootmiseks on vaja aminohapete skelette: selle ensüümi negatiivsed modulaatorid on seega indikaatorid hea energia kättesaadavusega (ATP, GTP ja NAD (P) H) ning positiivsete modulaatoritena süsteemid, mis näitavad energiavajadust (AMP, ADP, SKP, NAD (P) +, aminohapped ja kilpnäärmehormoonid).
Aminohapped (peamiselt leutsiin) on glutamaatdehüdrogenaasi positiivsed modulaatorid: kui tsütoplasmas on aminohappeid, saab neid kasutada valkude sünteesiks või need tuleb kõrvaldada, kuna neid ei saa koguneda (see selgitab, miks aminohapped on positiivsed modulaatorid) ).
Ammoniaagi kõrvaldamine: karbamiiditsükkel
Kalad utiliseerivad ammoniaagi, viies selle lõpuste kaudu vette; linnud muudavad selle kusihappeks (mis on kondensatsiooniprodukt) ja kõrvaldavad selle väljaheitega. Vaatame, mis juhtub inimestel: oleme öelnud, et glutamaatdehüdrogenaas muudab glutamaadi α- ketoglutaraati ja ammoniaaki, kuid me ei ole öelnud, et see esineb ainult maksa mitokondrites.
Mitokondriaalsed transaminaasid mängivad karbamiiditsükli kaudu ammoniaagi kõrvaldamise põhirolli.

Süsinikdioksiidi vesinikkarbonaatioonide (HCO3-) kujul aktiveerib biotiini kofaktor, moodustades karboksübiotiini, mis reageerib ammoniaagiga ja annab karbamiinhappe; järgmises reaktsioonis kasutatakse ATP-d fosfaadi ülekandmiseks karbamiinhappele, moodustades karbamüülfosfaadi ja ADP (ATP muundamine ADP -ks on karboksübiootiini saamise liikumapanev jõud.) Seda faasi katalüüsib karbamüülfosfaadi süntetaas ja esineb mitokondris. Karbamüülfosfaat ja ornitiin on ensüümi substraadid ornitiini trans -karbamülaas mis muudab need tsitrulliiniks; see reaktsioon esineb mitokondrites (hepatotsüütides). Toodetud tsitrulliin lahkub mitokondrist ja satub tsütoplasmas "toime" alla.arginiinsuktsinaadi süntetaas: toimub sulandumine tsitrulliini ja aspartaadi süsinikuskeleti vahel nukleofiilse rünnaku ja sellele järgneva vee eemaldamise teel. Arginiinsuktsinaadi süntetaasi ensüüm vajab ATP molekuli, nii et tekib energiline sidestus: ATP hüdrolüüs AMP -ks ja pürofosfaadiks (viimane muundatakse seejärel kaheks ortofosfaadi molekuliks) toimub molekuli d "vee väljutamisega substraadist. ja mitte söötme vee toimel.
"Järgmine ensüüm on"arginiini suktsinaas: see ensüüm suudab tsütoplasmas arginiinsuktsinaadi arginiiniks ja fumaraadiks jagada.
Ensüüm lõpetab karbamiiditsükli arginaassaadakse karbamiid ja ornitiin; karbamiid kõrvaldatakse neerude kaudu (uriin), samal ajal kui ornitiin naaseb mitokondrisse ja jätkab tsüklit.
Karbamiiditsüklit moduleerib arginiin kaudselt: arginiini kogunemine näitab, et karbamiiditsüklit tuleb kiirendada; arginiini moduleerimine on kaudne, kuna arginiin moduleerib positiivselt atsetüülglutamaadi süntetaasi ensüümi. Viimane on võimeline glutamaadi lämmastikule üle kandma atsetüülrühma: moodustub N-atsetüülglutamaat, mis on karbamüülfosfo süntetaasi ensüümi otsene modulaator.
Arginiin koguneb karbamiiditsükli metaboliidiks, kui ornamiini kõrvaldamiseks ei piisa karbamüülfosfaadi tootmisest.
Karbamiidi toodetakse ainult maksas, kuid on ka teisi saite, kus esmased reaktsioonid toimuvad.
Aju ja lihased kasutavad aminorühmade kõrvaldamiseks spetsiaalseid strateegiaid. Aju kasutab väga tõhusat meetodit, mille puhul kasutatakse ensüümi glutamiini süntetaas ja ensüüm glutamaas: esimene esineb neuronites, teine aga maksas. See mehhanism on väga tõhus kahel põhjusel:
Kaks aminorühma transporditakse ajust maksa ühe kandjaga;
Glutamiin on palju vähem toksiline kui glutamaat (glutamaat teostab ka neuronite ülekannet ega tohi ületada füsioloogilist kontsentratsiooni).
Kalade puhul toob sarnane mehhanism aminohapete aminorühma lõpustele.
Lihast (luustikust ja südamest) jõuavad aminorühmad maksa glükoosi-alaniini tsükli kaudu; kaasatud ensüüm on glutamiin-püruvaadi transaminaas: see võimaldab üle kanda aminorühmi (mis on glutamaadi kujul), muuta püruvaat alaniiniks ja samal ajal glutamaat lihastes a-ketoglutaraadiks ning katalüüsida vastupidine protsess maksas.
Erinevate ülesannete või positsioonidega transaminaasidel on ka struktuurilised erinevused ja need on elektroforeesi abil määratavad (neil on erinevad isoelektrilised punktid).
Transaminaaside olemasolu veres võib olla maksa- või südamekahjustuse sümptom (st maksa- või südamerakkude kudede kahjustus); transaminaasid on väga suurtes kontsentratsioonides nii maksas kui ka südames: elektroforeesi abil on võimalik kindlaks teha, kas kahjustus on tekkinud maksas või südamerakkudes.








-a-cosa-serve.jpg)