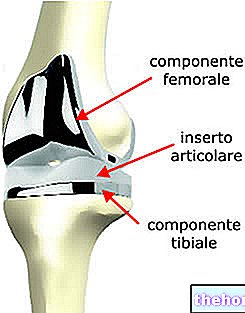
Toimeained: fluoksetiin
FLUOXEREN 20 MG KÕVAD KAPSLID
FLUOXEREN 20 mg / 5 ml suukaudne lahus
FLUOXEREN 20 MG JAOTATAVAD TABLETID
Näidustused Miks Fluoxereni kasutatakse? Milleks see mõeldud on?
FARMAKOTERAPEUTILINE KATEGOORIA
Antidepressandid. Selektiivsed serotoniini tagasihaarde inhibiitorid.
RAVI NÄIDUSTUSED
Depressiooni, obsessiiv -kompulsiivse häire ja buliimia ravi.
Vastunäidustused Fluoxeren'i ei tohi kasutada
Ülitundlikkus toimeaine või lõigus "Koostis" loetletud mis tahes abiainete suhtes.
Fluoksetiin on vastunäidustatud koos:
- pöördumatud ja mitteselektiivsed monoamiini oksüdaasi inhibiitorid (nt iproniasiid) (vt lõigud "Ettevaatusabinõud kasutamisel" ja "Koostoimed");
- südamepuudulikkuse korral kasutatav metoprolool (vt lõik "Koostoimed").
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Fluoxeren'i võtmist
Lapsed - alla 18 -aastased lapsed ja noorukid
Kliinilistes uuringutes täheldati antidepressantidega ravitud lastel ja noorukitel sagedamini suitsiidiga seotud käitumist (enesetapukatseid ja enesetapumõtteid) ja vaenulikkust (peamiselt agressiivsust, vastandlikku käitumist ja viha) kui platseebot saanud patsientidel.
Fluoxeren on ette nähtud kasutamiseks lastel ja noorukitel vanuses 8 kuni 18 aastat mõõduka kuni raske depressiooni episoodide raviks ning seda ei tohi kasutada muude näidustuste korral. Kui meditsiiniliste vajaduste põhjal otsustatakse ravi üle, tuleb patsienti hoolikalt jälgida enesetapumõjude ilmnemise suhtes. Lisaks on laste ja noorukite kohta saadaval ainult piiratud pikaajalised ohutusandmed, sealhulgas mõju kasvule, seksuaalsele küpsemisele ning kognitiivsele, emotsionaalsele ja käitumuslikule arengule (vt lõik 5.3).
19-nädalases kliinilises uuringus täheldati fluoksetiiniga ravitud lastel ja noorukitel pikkuse ja kehakaalu langust. Ei ole kindlaks tehtud, kas sellel on mõju normaalse pikkuse saavutamisele täiskasvanueas. Seda ei saa välistada. hilinenud puberteet (vt lõik "Kõrvaltoimed"). Seetõttu tuleb fluoksetiinravi ajal ja pärast seda jälgida puberteedi kasvu ja arengut (pikkus, kaal ja staadium vastavalt TANNERile).
Lastel läbi viidud uuringutes teatati sageli maaniast ja hüpomaaniast (vt lõik "Kõrvaltoimed"). Seetõttu on soovitatav regulaarselt jälgida maania / hüpomaania esinemist. Maniakaalsesse faasi siseneva patsiendi puhul tuleb fluoksetiinravi katkestada.
On oluline, et arst arutaks hoolikalt lapsega / noorukiga ja / või tema vanematega ravi riske ja kasu.
Krambid
Krambid kujutavad endast potentsiaalset riski antidepressantide kasutamisel. Seetõttu, nagu ka teiste antidepressantide puhul, tuleb fluoksetiini manustada ettevaatusega patsientidele, kellel on esinenud krampe. Ravi tuleb katkestada kõigil patsientidel, kellel esinevad krambid või kellel on täheldatud krampide esinemissageduse suurenemist. Ebastabiilsete krambihoogude / epilepsiaga patsientidel tuleb fluoksetiini manustamist vältida ja kontrollitud epilepsiaga patsiente tuleb hoolikalt jälgida (vt lõik "Koostoimed").
Elektrokonvulsioonravi (TEC)
TEC-ravi saavatel fluoksetiiniga ravitud patsientidel on harvadel juhtudel teatatud pikaajalistest krampidest, seetõttu on soovitatav olla ettevaatlik.
Mania
Antidepressante tuleb mania / hüpomaania anamneesiga patsientidel kasutada ettevaatusega.
Depressiooni all kannataval inimesel peaks ebanormaalselt ja püsivalt kõrgendatud meeleolu ilmnemine, mis on eufooriline, ebatavaliselt hea ja rõõmus ning avar või ärrituv, ajendama patsienti oma arstiga nõu pidama. Nagu kõigi antidepressantide puhul, tuleb fluoksetiini kasutamine lõpetada niipea, kui patsiendil tekivad maania sümptomid.
Maksa / neerufunktsioon
Fluoksetiin metaboliseerub ulatuslikult maksas ja eritub neerude kaudu. Olulise maksafunktsiooni häirega patsientidel on soovitatav kasutada väiksemat annust, nt. üks manustamine igal teisel päeval. Kui fluoksetiini manustati 2 kuu jooksul annustes 20 mg ööpäevas, olid raske neerukahjustusega patsiendid (GFR dialüüs ei näidanud erinevusi fluoksetiini ega norfluoksetiini plasmatasemes võrreldes normaalse neerufunktsiooniga kontrollrühmaga).
Tamoksifeen
Fluoksetiin, mis on tugev CYP2D6 inhibiitor, võib vähendada endoksifeeni, mis on üks olulisemaid tamoksifeeni aktiivseid metaboliite, kontsentratsiooni. Seetõttu tuleb võimaluse korral vältida tamoksifeenravi ajal fluoksetiini manustamist (vt lõik "Koostoimed").
Kardiovaskulaarsed mõjud
Ägeda südamehaiguse kliiniline kogemus on piiratud, seetõttu tuleb fluoksetiini kasutamisel olla ettevaatlik. Fluoksetiini tuleb ettevaatusega kasutada ka patsientidel, kellel on sellised haigused nagu kaasasündinud pika QT sündroom, QT -intervalli pikenemine perekonnas või muud arütmiale eelsoodumusega kliinilised seisundid (nt hüpokaleemia, hüpomagneseemia, bradükardia, äge müokardiinfarkt või dekompenseeritud südamepuudulikkus) või fluoksetiin (nt maksapuudulikkus).
Stabiilse südamehaigusega patsientidel tuleb enne ravi alustamist kaaluda EKG -d (elektrokardiogrammi).
Kui fluoksetiinravi ajal ilmnevad südame rütmihäire nähud, tuleb ravi katkestada ja teha EKG.
Diabeet
Diabeediga patsientidel võib SSRI -ravi muuta glükeemilist kontrolli. Hüpoglükeemia tekkis fluoksetiinravi ajal, samas kui hüperglükeemia tekkis pärast ravimi kasutamise lõpetamist. Vajalikuks võib osutuda insuliini ja / või suukaudse hüpoglükeemilise aine annuse kohandamine.
Enesetapp / enesetapumõtted või kliiniline halvenemine
Depressioon on seotud enesetapumõtete, enesevigastamise ja enesetapu (suitsiidiga seotud sündmused) suurenenud riskiga ning see risk püsib kuni olulise remissiooni tekkimiseni. Kuna paranemine ei pruugi ilmneda ravi esimestel nädalatel või kauem, tuleb patsiente tähelepanelikult jälgida kuni paranemiseni. On tavaline kliiniline kogemus, et enesetapurisk võib paranemisprotsessi alguses suureneda.
Teised psühhiaatrilised seisundid, mille puhul Fluoxeren on ette nähtud, võivad samuti olla seotud suitsiidikäitumise suurenenud riskiga. Lisaks võib neid seisundeid seostada raske depressiivse häirega. Järelikult tuleb järgida samu ettevaatusabinõusid, mida järgitakse raske depressiooniga patsientide ravimisel ka teiste psühhiaatriliste häiretega patsientide ravimisel.
Patsientidel, kellel on anamneesis suitsiidiga seotud juhtumeid või kellel esineb enne ravi alustamist märkimisväärne enesetapumõte, on suurem risk enesetapumõtete või enesetapukatse tekkeks ning neid tuleb ravi ajal hoolikalt jälgida. psühhiaatriliste häiretega täiskasvanud patsientidel, kes said antidepressante, on näidanud, et alla 25 -aastastel antidepressantidega ravitud patsientidel on suitsiidikäitumise risk suurenenud võrreldes platseeboga.
Ravi ajal, eriti ravi alguses ja pärast annuse muutmist, on vajalik patsientide, eriti kõrge riskiga patsientide hoolikas jälgimine. Patsiente (ja nende hooldajaid) tuleb teavitada vajadusest kontrollida kliinilist halvenemist, enesetapumõjude ilmnemist. käitumist või mõtteid ning ebatavalisi muutusi käitumises ning nende sümptomite ilmnemisel pöörduge kohe oma arsti poole.
Akatisia / psühhomotoorne rahutus
Fluoksetiini kasutamist on seostatud akatiisia tekkega, mida iseloomustab subjektiivselt ebameeldiv või valulik rahutustunne ja psühhomotoorne erutus, millega sageli kaasneb võimetus rahulikult istuda. See juhtub kõige tõenäolisemalt ravi esimestel nädalatel. Nende sümptomitega patsientidel võib annuse suurendamine olla kahjulik.
Pärast SSRI -ravi lõpetamist täheldati võõrutusnähte
Täheldatud katkestamissümptomid on ravi lõpetamisel tavalised, eriti kui ravi lõpetatakse järsult (vt lõik "Kõrvaltoimed").
Kliinilistes uuringutes esines ravi katkestamisel täheldatud kõrvaltoimeid 60% -l patsientidest nii fluoksetiini kui ka platseebo rühmas. Nendest kõrvaltoimetest olid 17% fluoksetiinirühmas ja 12% fluoksetiinigrupis platseebost rasked.
Võõrutusnähtude risk võib sõltuda mitmest tegurist, sealhulgas ravi kestusest, annusest ja annuse vähendamise kiirusest.
Kõige sagedamini teatatud reaktsioonid on pearinglus, sensoorsed häired (sh paresteesia), unehäired (sh unetus ja intensiivsed unenäod), asteenia, erutus või ärevus, iiveldus ja / või oksendamine, värisemine ja peavalu. Üldiselt on nende sümptomite intensiivsus kerge kuni mõõdukas, kuid mõnel patsiendil võivad need olla rasked. Need ilmnevad tavaliselt esimese paari päeva jooksul pärast ravi lõpetamist. Üldiselt on need sümptomid iseenesest mööduvad ja kaovad tavaliselt kahe nädala jooksul. see võib kesta kauem (2-3 kuud või kauem). Seetõttu on soovitatav ravi lõpetamisel Fluoxeren'i annust järk-järgult vähendada, vähemalt 1 ... 2 nädala jooksul, olenevalt patsiendi vajadustest (vt lõik "Annustamine , manustamisviis ", Fluoxeren -ravi lõpetamisel täheldatud katkestamise sümptomid).
Verejooks
SSRI -de kasutamisel on teatatud nahaverejooksu ilmingutest, nagu ekhümoos ja purpur. Fluoksetiinravi ajal on harva esinenud ekhümoosi. Harva on teatatud muudest hemorraagilistest ilmingutest (nt günekoloogilised verejooksud, seedetrakti verejooks ja muu naha- või limaskestaverejooks). SSRI -sid kasutavatel patsientidel on soovitatav olla ettevaatlik, eriti samaaegsel kasutamisel. suukaudsed antikoagulandid, trombotsüütide funktsiooni mõjutavad ravimid või muud ravimid, mis võivad suurendada verejooksu riski (nt ebatüüpilised antipsühhootikumid, nagu klosapiin, fenotiasiinid, enamik tritsüklilistest antidepressantidest, aspiriin, MSPVA -d), samuti patsiendid, kellel on anamneesis patoloogilistest ilmingutest, mida iseloomustab verejooks (vt lõik "Koostoimed").
Müdriaas
Fluoksetiiniga seoses on teatatud müdriaasist; Seetõttu tuleb olla ettevaatlik fluoksetiini määramisel kõrgendatud silmasisese rõhuga või ägeda kitsanurga glaukoomi riskiga patsientidele.
Naistepuna
Selektiivsete serotoniini tagasihaarde inhibiitorite ja naistepuna (Hypericum perforatum) sisaldavate taimsete preparaatide samaaegsel kasutamisel võivad tekkida tugevamad serotoniinergilised toimed, näiteks serotoniinisündroom.
Serotoniini sündroom või pahaloomulise neuroleptilise sündroomi sarnased sündmused
Harvadel juhtudel on seoses fluoksetiinraviga teatatud serotoniinisündroomi või pahaloomulise neuroleptilise sündroomi sarnaste sündmuste tekkest, eriti kui fluoksetiini manustatakse koos teiste serotoniinergiliste ravimitega (muuhulgas L-trüptofaan) ja / või neuroleptikumidega (vt. "Koostoimed"). Kuna need sündroomid võivad tekitada patsiendile potentsiaalselt eluohtlikke seisundeid, võivad selliste nähtude ilmnemisel tekkida (neid iseloomustavad mitmed sümptomid nagu hüpertermia, jäikus, müokloonus, autonoomse närvisüsteemi ebastabiilsus koos võimalike kiirete elutähtsate kõikumistega, vaimne seisund, sealhulgas segasus, ärrituvus ja äärmine erutus kuni deliiriumi ja koomani), tuleb fluoksetiinravi katkestada ja alustada sümptomaatilist toetavat ravi.
Pöördumatud mitteselektiivsed monoamiini oksüdaasi inhibiitorid (nt iproniasiid)
On teatatud tõsistest ja mõnikord surmaga lõppevatest reaktsioonidest patsientidel, kes kasutasid SSRI-d koos mitteselektiivse pöördumatu monoamiini oksüdaasi inhibiitoriga (MAOI).
Nendel juhtudel on serotoniinisündroomiga sarnased tunnused ja neid võib segi ajada (või diagnoosida) pahaloomulise neuroleptilise sündroomiga. Tsüproheptadiinist või dantroleenist võib selliste reaktsioonidega patsientidele kasu olla. Ravimi koostoime sümptomid MAOI -ga on järgmised: hüpertermia, jäikus, müokloonus, autonoomne ebastabiilsus koos võimalike kiirete elutähtsate kõikumistega, vaimse seisundi muutused, sealhulgas segasus, ärrituvus ja äärmine erutus kuni deliiriumi ja koomani.
Seetõttu on fluoksetiin vastunäidustatud kombinatsioonis pöördumatu mitteselektiivse MAOI-ga (vt lõik "Vastunäidustused"). Kuna viimase toime kestab 2 nädalat, tuleb fluoksetiinravi alustada alles 2 nädalat pärast pöördumatu mitteselektiivse MAOI lõpetamist. Samamoodi peaks enne fluoksetiinravi lõpetamist mööduma vähemalt 5 nädalat, enne kui alustatakse ravi pöördumatu mitteselektiivse selektiivne MAOI.
Koostoimed Millised ravimid või toidud võivad muuta Fluoxereni toimet
Rääkige oma arstile või apteekrile, kui olete hiljuti kasutanud mingeid muid ravimeid, isegi ilma retseptita.
Koostoimeuuringuid on läbi viidud ainult täiskasvanutel.
Vastunäidustatud ühendused
Pöördumatud mitteselektiivsed monoamiini oksüdaasi inhibiitorid (nt iproniasiid)
On teatatud tõsistest ja mõnikord surmavatest reaktsioonidest patsientidel, kes kasutasid SSRI-d koos pöördumatu mitteselektiivse monoamiini oksüdaasi inhibiitoriga (MAOI).
Nendel juhtudel on serotoniinisündroomile sarnased tunnused ja neid võib segi ajada (või diagnoosida) pahaloomulise neuroleptilise sündroomiga.
Tsüproheptadiinist või dantroleenist võib selliste reaktsioonidega patsientidele kasu olla. Ravimi koostoime sümptomid MAOI -ga on järgmised: hüpertermia, jäikus, müokloonus, autonoomne ebastabiilsus koos võimalike kiirete elutähtsate kõikumistega, vaimse seisundi muutused, sealhulgas segasus, ärrituvus ja äärmine erutus kuni deliiriumi ja koomani.
Seetõttu on fluoksetiin vastunäidustatud kombinatsioonis pöördumatu mitteselektiivse MAOI-ga (vt lõik "Vastunäidustused"). Kuna viimase toime kestab 2 nädalat, tuleb fluoksetiinravi alustada alles 2 nädalat pärast pöördumatu mitteselektiivse MAOI lõpetamist. Samamoodi peaks enne fluoksetiinravi katkestamist mööduma vähemalt 5 nädalat enne ravi alustamist pöördumatu mitteselektiivse selektiivne MAOI.
Südamepuudulikkuse korral kasutatav metoprolool: metoproloolist põhjustatud kõrvaltoimete, sealhulgas liigse bradükardia risk võib suureneda selle metabolismi pärssimise tõttu fluoksetiini poolt (vt lõik "Vastunäidustused").
Kombinatsioone ei soovitata
Tamoksifeen: Kirjanduses on kirjeldatud farmakokineetilist koostoimet CYP2D6 inhibiitorite ja tamoksifeeni vahel, kusjuures ühe kõige aktiivsema tamoksifeenivormi ehk endoksifeeni plasmakontsentratsioon väheneb 65-75%. Mõnedes uuringutes on teatatud tamoksifeeni efektiivsuse vähenemisest, mida manustatakse samaaegselt mõne SSRI antidepressandiga. Kuna seda ei saa välistada, tuleb võimalusel vältida tugevate CYP2D6 inhibiitorite (sh fluoksetiini) samaaegset manustamist (vt. jaotis "Ettevaatusabinõud kasutamisel").
Alkohol: rutiinsetes testides ei põhjusta fluoksetiin vere alkoholisisalduse tõusu ega võimenda alkoholi toimet. SSRI ja alkoholravi kombinatsioon ei ole siiski soovitatav.
MAOI-tüüp A, sealhulgas linesoliid ja metüültioniiniumkloriid (metüleensinine): serotoniinisündroomi, sealhulgas kõhulahtisuse, tahhükardia, higistamise, värisemise, segasuse või kooma oht. Kui nende toimeainete samaaegset kasutamist koos fluoksetiiniga ei saa vältida, tuleb hoolikalt jälgida kliinilist seisundit ja alustada samaaegsete ravimite manustamist võimalikult väikeste soovitatud annustega (vt lõik 4.4).
Mekitasiin: Flukoksetiin võib metabolismi pärssimise tõttu suurendada mekvitasiini kõrvaltoimete riski (nt QT -intervalli pikenemine).
Ettevaatust nõudvad ühendused
Fenütoiin: Fluoksetiiniga kombineerituna on täheldatud muutusi veres. Mõnel juhul on esinenud toksilisuse ilminguid. Seetõttu on soovitatav manustada samaaegselt kasutatavat ravimit vastavalt konservatiivsetele raviskeemidele ja hoolikalt jälgida patsiendi kliinilisi seisundeid.
Serotoniinergilised ravimid (liitium, tramadool, triptaanid, trüptofaan, selegiliin (MAOI-tüüp B), naistepuna (Hypericum perforatum)): on teatatud kergest serotoniinisündroomist pärast SSRI-de manustamist koos ravimitega, millel on ka " Seepärast tuleb fluoksetiini samaaegselt kasutada nende ravimitega ettevaatlikult, sihipärasemalt ja sagedamini kliiniliselt jälgides (vt lõik "Ettevaatusabinõud kasutamisel"). Kombinatsioon triptaanidega suurendab täiendavat riski koronaarsete veresoonte ahenemise ja hüpertensiooni tekkeks.
QT -intervalli pikenemine: Kuigi fluoksetiini ja teiste QT -intervalli pikendavate ravimite kombinatsiooni kohta ei ole kliinilisi uuringuid läbi viidud, ei saa välistada fluoksetiini ja nende ravimite koostoimet. Järelikult võib fluoksetiini ja QT -intervalli pikendavate ravimite samaaegset manustamist välistada. intervall - nagu IA ja III klassi antiarütmikumid, antipsühhootikumid (nt fenotiasiini derivaadid, pimosiid, haloperidool), tritsüklilised antidepressandid, mõned antimikroobsed ained (nt sparfloksatsiin, moksifloksatsiin, erütromütsiin IV, pentamidiin), malaariavastased ained, eriti antihistamiinikumid, ) - nõuab ettevaatust (vt lõigud "Ettevaatusabinõud kasutamisel", "Kõrvaltoimed" ja "Üleannustamine").
Hemostaasi mõjutavad ravimid (suukaudsed antikoagulandid, olenemata nende toimemehhanismist, trombotsüütide vastased ained, sh aspiriin ja MSPVA -d): suurenenud verejooksu oht. Kliiniline jälgimine ja sagedasem INR -i jälgimine tuleb läbi viia suukaudsete antikoagulantidega. Annuse kohandamine võib osutuda vajalikuks fluoksetiinravi ajal ja pärast selle lõpetamist (vt lõigud "Ettevaatusabinõud kasutamisel" ja "Kõrvaltoimed").
Tsüproheptadiin: üksikjuhtudel on teatatud fluoksetiini antidepressantide aktiivsuse vähenemisest, kui seda kasutatakse koos tsüproheptadiiniga.
Hüponatreemiat esile kutsuvad ravimid: Hüponatreemia on fluoksetiini soovimatu toime.
Kasutamine koos teiste hüponatreemiaga seotud ainetega (nt diureetikumid, desmopressiin, karbamasepiin ja okskarbasepiin) võib suurendada riski (vt lõik "Kõrvaltoimed").
Ravimid, mis alandavad krampide läve, on fluoksetiini soovimatu toime. Riski võib suurendada, kui seda kasutatakse koos teiste ravimitega, mis on võimelised alandama krampide läve (nt TCA, teised SSRI -d, fenotiasiinid, butürofenoonid, meflokviin, klorokiin, buproprioon, tramadool).
Muud ravimid, mida metaboliseerib CYP2D6: fluoksetiin on tugev ensüümi CYP2D6 inhibiitor, seetõttu võib samaaegne ravi ravimitega, mida samuti see ensüümsüsteem metaboliseerib, põhjustada ravimite koostoimeid, eriti kitsa terapeutilise indeksiga ravimite (flekainiid, enkainiid, propafenoon ja nebivolool) ja tiitritud ravimeid, aga ka koos atomoksetiini, karbamasepiini, tritsükliliste antidepressantide ja risperidooniga. Nende manustamist tuleb alustada või kohandada alates annuste vahemiku madalaimast väärtusest. Seda tuleb teha ka siis, kui olete viimase 5 nädala jooksul võtnud fluoksetiini.
Hoiatused Oluline on teada, et:
Kaalukaotus
Fluoksetiini võtvatel patsientidel võib tekkida kehakaalu langus, kuigi see langus on tavaliselt proportsionaalne kehakaalu algusega.
Nahalööve ja allergilised reaktsioonid
On teatatud lööbest, anafülaktoidsetest sündmustest ja progresseeruvatest süsteemsetest sündmustest, mõnikord tõsistest (naha, neerude, maksa ja kopsude puhul). Patsient peab oma arsti viivitamatult teavitama nahalööbe ja / või nõgestõve ilmnemisest või muudest allergilistest ilmingutest, mis võivad tekkida hingamisraskustega (vt „Kõrvaltoimed“). Nahalööbe või muude allergiliste nähtude korral, mille puhul ei ole võimalik kindlaks teha erinevat etioloogiat, tuleb fluoksetiini manustamine katkestada.
Viljakus, rasedus ja imetamine
Rasedus
Kui te olete rase, imetate või arvate end olevat rase või kavatsete rasestuda, pidage enne selle ravimi kasutamist nõu oma arstiga.
Mõned epidemioloogilised uuringud näitavad fluoksetiini kasutamise esimesel trimestril suurenenud kardiovaskulaarsete defektide riski. Mehhanism on teadmata. Üldiselt näitavad andmed, et pärast emade fluoksetiiniga kokkupuudet on vastsündinu risk kardiovaskulaarse defektiga.
Üldpopulatsioonis on umbes üks laps sajast sündinud südamepuudulikkusega; fluoksetiini kasutavatel emadel suureneb see protsent 2 -le 100 -st.
Epidemioloogilised andmed on näidanud, et SSRI -de kasutamine raseduse ajal, eriti raseduse hilises staadiumis, võib suurendada vastsündinu püsiva pulmonaalse hüpertensiooni (PPHN) riski.
Lisaks, kuigi fluoksetiini võib raseduse ajal kasutada, tuleb olla ettevaatlik, eriti raseduse lõpus või vahetult enne sünnituse algust, sest vastsündinutel on täheldatud järgmisi toimeid: ärrituvus, värin, hüpotoonia, püsiv nutt, imemisraskused või magamine. Need sümptomid võivad viidata nii serotonergilisele toimele kui ka võõrutussündroomile. Nende sümptomite ilmnemise aeg ja kestus võivad olla seotud fluoksetiini ja selle aktiivse metaboliidi norfluoksetiini (4–6 päeva) pika poolväärtusajaga. 16 päeva).
Toitmisaeg
On teada, et fluoksetiin ja selle aktiivne metaboliit norfluoksetiin erituvad inimese rinnapiima. Kui ravi fluoksetiiniga peetakse vajalikuks, tuleb kaaluda rinnaga toitmise katkestamist, kuid kui rinnaga toitmist jätkatakse, tuleb määrata madalaim efektiivne fluoksetiini annus.
Viljakus
Loomkatsed on näidanud, et fluoksetiin võib mõjutada sperma kvaliteeti. Inimeste juhtumite aruanded mõnede SSRI -dega on näidanud, et mõju sperma kvaliteedile on pöörduv. Mõju inimese viljakusele ei ole seni täheldatud.
Toime autojuhtimise ja masinate käsitsemise võimele
Fluoxeren ei mõjuta või mõjutab ebaoluliselt autojuhtimise ja masinate käsitsemise võimet. Patsiendid peaksid vältima sõiduki juhtimist või ohtlike masinatega töötamist, kuni nad on piisavalt kindlad, et nende võimed ei ole halvenenud.
Oluline teave mõne koostisosa kohta
FLUOXEREN 20 mg / 5 ml suukaudne lahus sisaldab sahharoosi. Kui arst on teile öelnud, et te ei talu teatud suhkruid, võtke enne selle ravimi kasutamist ühendust oma arstiga.
FLUOXEREN 20 mg dispergeeruvad tabletid sisaldavad sorbitooli. Kui arst on teile öelnud, et te ei talu teatud suhkruid, võtke enne selle ravimi kasutamist ühendust oma arstiga.
Annustamine ja kasutusviis Fluoxereni kasutamine: Annustamine
Suukaudseks manustamiseks.
Peamised depressiooni episoodid
Täiskasvanud ja eakad: soovitatav annus on 20 mg ööpäevas (1 kõvakapsel või 1 dispergeeruv tablett või 5 ml suukaudset lahust). Vajadusel tuleb annust muuta või kohandada 3 ... 4 nädala jooksul pärast ravi alustamist ja seejärel vastavalt kliinilisele vajadusele. Kuigi suuremate annuste korral võib mõnedel patsientidel, kellel 20 mg annus on ebapiisav, tekkida kõrvaltoimete oht annust võib järk -järgult suurendada kuni maksimaalse 60 mg -ni. Iga patsiendi jaoks tuleb annust kohandada ettevaatlikult, et hoida patsiente väikseima efektiivse annusena.
Depressiooniga patsiente tuleb ravida piisavalt, vähemalt 6 kuud, et tagada sümptomite puudumine.
Obsessiiv-kompulsiivne häire
Täiskasvanud ja eakad: soovitatav annus on 20 mg ööpäevas (1 kõvakapsel või 1 dispergeeruv tablett või 5 ml suukaudset lahust). Kuigi suuremate annuste korral võib esineda kõrvaltoimete esinemissageduse suurenemist, võib ebapiisava ravivastuse korral pärast 2 -nädalast ravi annusega 20 mg suurendada seda maksimaalselt 60 mg -ni. Kui 10 nädala jooksul paranemist ei täheldata, tuleb fluoksetiinravi uuesti kaaluda. Kui on saavutatud hea ravivastus, võib ravi jätkata individuaalselt kohandatud annusega. Kuigi süstemaatilisi uuringuid fluoksetiinravi jätkamise aja määramiseks ei ole läbi viidud, on OCD krooniline haigus ja ravile alluvatel patsientidel on mõistlik kaaluda ravi pikendamist üle 10 nädala. Iga patsiendi jaoks tuleb annuseid hoolikalt muuta, et patsient saaks väikseima efektiivse annuse.Ravi vajadust tuleb perioodiliselt uuesti hinnata. Mõned arstid peavad samaaegset käitumuslikku psühhoteraapiat kasulikuks patsientidele, kes on ravile hästi reageerinud.
Pikaajalist efektiivsust (üle 24 nädala) ei ole OCD puhul tõestatud.
Buliimia
Täiskasvanud ja eakad: soovitatav annus on 60 mg päevas ühekordse suukaudse manustamisena hommikul (3 kõvakapslit või 3 dispergeeruvat tabletti või 15 ml suukaudset lahust). Efektiivsust ei ole tõestatud bulimia nervosa korral. tähtaeg (üle 3 kuu).
Täiskasvanud - kõigi näidustuste korral
Soovitatavat annust võib suurendada või vähendada. Üle 80 mg ööpäevaseid annuseid ei ole süstemaatiliselt hinnatud.
Fluoksetiini võib manustada ühe või mitme annusena, koos toiduga või ilma.
Kui ööpäevane annus ületab 20 mg, soovitatakse FLUOXEREN'i manustada kaks korda päevas, hommiku- ja lõunasöögi ajal.
Kui annustamine lõpetatakse, püsivad farmakoloogiliselt aktiivsed ained kehas nädalaid, mida tuleb ravi alustamisel või lõpetamisel arvesse võtta.
Kapsel ja vedelad vormid on bioekvivalentsed.
8 -aastased ja vanemad lapsed ja noorukid (mõõdukas kuni raske raske depressiooni episood)
Ravi tuleb alustada ja jälgida spetsialisti järelevalve all. Algannus on 10 mg ööpäevas, manustatuna 2,5 ml Fluoxereni suukaudse lahusena. Annust tuleb kohandada ettevaatlikult ja individuaalselt, et hoida patsient väikseima efektiivse annusena.
1-2 nädala pärast võib annust suurendada 20 mg -ni päevas. Kliiniline kogemus üle 20 mg ööpäevaste annuste kasutamisel on minimaalne. Üle 9 nädala kestnud ravi kohta on andmed piiratud.
Madala kehakaaluga lapsed
Vähendatud kehakaaluga laste kõrgema plasmataseme tõttu saab terapeutilise toime saavutada väiksemate annustega.
Ravile alluvate pediaatriliste patsientide puhul tuleb uuesti hinnata vajadust jätkata ravi 6 kuu pärast. Kui 9 nädala jooksul ei saavutata kliinilist kasu, tuleb ravi uuesti läbi vaadata.
Eakad kodanikud
Annuse suurendamisel on soovitatav olla ettevaatlik ja üldiselt ei tohi päevane annus ületada 40 mg. Maksimaalne soovitatav annus on 60 mg päevas. Ettevaatus on soovitatav eakatel patsientidel, kellel on samaaegsed süsteemsed haigused või kes kasutavad muid ravimeid.
Maksapuudulikkusega patsientidel või patsientidel, kellel on võimalik "koostoime Fluoxereni ja samaaegselt kasutatavate ravimite vahel", tuleb kaaluda väiksema või harvema annuse (nt 20 mg igal teisel päeval) manustamist (vt lõik "Koostoimed").
Vähenenud maksa- või neerufunktsiooniga isikutel ning eakatel, kaasuvate haigustega või teisi ravimeid kasutavatel isikutel tuleb FLUOXEREN'i annust vastavalt vähendada või annustevahelist intervalli suurendada (nt 20 mg igal teisel päeval).
Pärast Fluoxeren -ravi lõpetamist täheldati võõrutusnähte
Ravi järsku katkestamist tuleks vältida. Fluoxeren-ravi katkestamisel tuleb annust järk-järgult vähendada vähemalt 1-2 nädala jooksul, et vähendada võõrutusreaktsioonide riski (vt lõigud "Ettevaatusabinõud kasutamisel") ja "Kõrvaltoimed" ").
Kui pärast annuse vähendamist või ravi katkestamist tekivad talumatud sümptomid, võib kaaluda eelnevalt määratud annuse jätkamist. Seejärel võib arst jätkata annuse vähendamist, kuid järk -järgult.
Arsti soovitatud FLUOXEREN lahuse täpse annuse saab hõlpsasti järgida, järgides alltoodud juhiseid:
- Sisestage doseerimispipett pudelisse, veendudes, et kolb on lõpuni sisestatud;
- Tõmmake kolbi ülespoole, kuni saavutatakse arsti soovitatud annus;
- Valage sisu klaasi ja lahjendage veega maitse järgi.
FLUOXEREN dispergeeruvad tabletid võib alla neelata ilma närimiseta või lahustada vees, lahjendades vastavalt soovile.
Üleannustamine Mida teha, kui olete võtnud liiga palju Fluoxeren'i
FLUOXERENi ülemäärase annuse juhusliku allaneelamise / võtmise korral teavitage sellest kohe oma arsti või minge lähimasse haiglasse. Kui teil on lisaküsimusi FLUOXERENi kasutamise kohta, pidage nõu oma arsti või apteekriga.
Sümptomid
Fluoksetiinist tingitud üleannustamise juhtumid on tavaliselt kerged. Üleannustamise sümptomiteks on iiveldus, oksendamine, krambid, muutuvad kardiovaskulaarsed düsfunktsioonid asümptomaatiliste arütmiate tõttu (sh sõlme rütmi rütmihäired ja ventrikulaarsed arütmiad) või EKG muutused, mis viitavad QT -intervalli pikenemisele kuni südame seiskumiseni, kopsufunktsiooni häire ja kesknärvisüsteemi muutuse sümptomid erutus koomasse. Fluoksetiini üleannustamise tõttu on surmav tulemus olnud äärmiselt haruldane.
Ravi
Soovitatav on südamefunktsiooni ja eluliste näitajate jälgimine ning üldised sümptomaatilised ja toetavad meetmed. Spetsiifilisi antidoote pole teada.
Sunnitud diurees, dialüüs, hemoperfusioon ja asendusülekanne tõenäoliselt kasu ei too. Aktiivsüsi, mida saab kasutada koos sorbitooliga, võib olla isegi tõhusam ravi kui oksendamine või maoloputus. Üleannustamise ravimisel kaaluge mitmete ravimite kaasamise võimalust. Patsiendid, kes on võtnud liiga palju tritsüklilist antidepressanti, võivad vajada pikemat aega hoolikaks arstlikuks jälgimiseks, kui nad võtavad või on hiljuti kasutanud fluoksetiini.
JÄRGMINE HALDUS: TAGASISÜNDROOM. Juhuslikul ühe või mitme annuse võtmata jätmisel on võõrutussündroomi tekkimise oht minimaalne.
Kõrvaltoimed Millised on Fluoxereni kõrvaltoimed
Nagu kõik ravimid, võib ka FLUOXEREN põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki.
Ohutusprofiili kokkuvõte
Kõige sagedamini teatatud kõrvaltoimed fluoksetiiniga ravitud patsientidel olid peavalu, iiveldus, unetus, väsimus ja kõhulahtisus. Kõrvaltoimete intensiivsus ja esinemissagedus võivad ravi jätkudes väheneda ega vaja tavaliselt ravi katkestamist.
Kõrvaltoimete tabel
Allolevas tabelis on toodud kõrvaltoimed, mida täheldati flueksetiinravi ajal täiskasvanutel ja lastel. Mõned neist kõrvaltoimetest on tavalised ka teiste SSRI -de puhul.
Allpool esitatud sagedused arvutati täiskasvanute kliiniliste uuringute (n = 9297) ja spontaansete aruannete põhjal.
Hinnanguline esinemissagedus: väga sage (≥ 1/10); sage (≥ 1/100 kuni
- Trombotsütopeenia
- Neutropeenia
- Leukopeenia
- Anafülaktiline reaktsioon
- Seerumi haigus
- Antidiureetilise hormooni sobimatu sekretsioon
- Söögiisu vähenemine 1
- Hüponatreemia
- Unetus 2
- Ärevus
- Närvilisus
- Rahutus
- Pinge
- Vähenenud libiido 3
- Unehäired
- Ebanormaalsed unenäod 4
- Depersonaliseerimine
- Kõrgendatud meeleolu
- Eufooriline meeleolu
- Ebanormaalne mõtlemine
- Ebanormaalne orgasm 5
- Bruksism
- Suitsidaalne mõtlemine ja käitumine 6
- Hüpomaania
- Mania
- Hallutsinatsioonid
- Erutus
- Paanikahood
- Segadusseisund
- Düsfeemia agressioon
- Peavalu
- Tähelepanuhäired
- Pearinglus
- Düsgeusia
- Letargia
- Unisus 7
- Värin
- Psühhomotoorne hüperaktiivsus
- Düskineesia
- Ataksia
- Tasakaalu häired
- Müokloonus
- Mälu halvenemine
- Krambid
- Akatisia
- Buccolingual sündroom
- Serotoniini sündroom
- Ähmane nägemine
- Müdriaas
- Tinnitus
- Südamepekslemine
- Ventrikulaarne arütmia, sealhulgas torsades de pointes
- QT -intervalli pikenemine EKG -s
- Punetus 8
- Hüpotensioon
- Vaskuliit
- Vasodilatatsioon
- Haigutama
- Hingeldus
- Ninaverejooks
- Farüngiit
- Kopsupatoloogiad (põletikulised protsessid, millel on erinev histopatoloogia ja / või fibroos) 9
- Kõhulahtisus
- Iiveldus
- Ta tõmbus tagasi
- Düspepsia
- Kuiv suu
- Düsfaagia
- Seedetrakti verejooks 10
- Söögitoru valu
- Idiosünkraatiline hepatiit
- Nahalööve 11
- Urtikaaria
- Sügelus
- Hüperhidroos
- Alopeetsia
- Suurenenud kalduvus verevalumitele
- Külm higi
- Angioödeem
- Verevalumid
- Valgustundlikkus
- Lilla
- Multiformne erüteem
- Stevensi-Johnsoni sündroom
- Toksiline epidermaalne nekrolüüs (Lyelli sündroom)
- Artralgia
- Lihaste kokkutõmbed
- Müalgia
- Sage urineerimine 12
- Düsuuria
- Kusepeetus
- Urineerimishäire
- Günekoloogiline verejooks 13
- Erektsioonihäired
- Ejakulatsioonihäire 14
- Seksuaalne düsfunktsioon
- Galaktorröa
- Hüperprolaktineemia
- Priapism
- Väsimus 15
- Närviline tunne
- Külmavärinad
- Halb enesetunne
- Kummaline tunne
- Külm tunne
- Kuum tunne
- Limaskestade verejooks
- Kaalukaotus
- Transaminaaside aktiivsuse suurenemine
- Suurenenud gammaglutamüültransferaas
1 Kaasa arvatud anoreksia
2 Sisaldab varajast ärkamist hommikul, esmast unetust, vahepealset unetust
3 Sisaldab libiido kaotust
4 Sisaldab õudusunenägusid
5 Sisaldab anorgasmiat
6 Hõlmab lõpetatud enesetappu, enesetapumõtet, tahtlikku enesevigastamist, enesevigastamist, enesetapukäitumist, enesetapumõtteid, enesetapukatse, haigeid mõtteid, enesevigastamist. Need sümptomid võivad olla põhjustatud haigusest.
7 Kaasa arvatud hüpersomnia, sedatsioon
8 Sisaldab kuumahooge
9 Hõlmab atelektaasi, interstitsiaalset kopsuhaigust, kopsupõletikku
10 Hõlmab peamiselt igemete verejooksu, hememeeset, hematokeesiat, rektaalset verejooksu, hemorraagilist kõhulahtisust, melaenat ja maohaavandi verejooksu
11 Kaasa arvatud erüteem, eksfoliatiivne lööve, kuumalööve, lööve, erüteemiline lööve, follikulaarne lööve, generaliseerunud lööve, makulaarne lööve, makulopapulaarne lööve, morbilliformne lööve, papulaarne lööve, sügelev lööve, vesikulaarne lööve, erütematoosne lööve
12 Kaasa arvatud pollakiuria
13 Hõlmab emakakaela verejooksu, emaka düsfunktsiooni, emaka verejooksu, suguelundite verejooksu, menometrorraagiat, menorraagiat, metrorraagiat, polümenorröad, menopausijärgset verejooksu, emaka verejooksu, tupeverejooksu
14 Hõlmab ejakulatsiooni ebaõnnestumist, ejakulatsiooni düsfunktsiooni, enneaegset seemnepurset, hilinenud ejakulatsiooni, retrograadset ejakulatsiooni
15 Kaasa arvatud asteenia.
Samuti on teatatud maitsehäiretest, pearinglusest, eufooriast, anorgasmiast ja hüponatreemiast.
Valitud kõrvaltoimete kirjeldus
Enesetapp / enesetapumõtted või kliiniline halvenemine: Fluoksetiinravi ajal või varsti pärast ravi lõpetamist on teatatud enesetapumõtete ja suitsidaalse käitumise juhtudest (vt lõik "Ettevaatusabinõud kasutamisel").
Luumurrud: Epidemioloogilised uuringud, mis viidi läbi peamiselt 50 -aastastel ja vanematel patsientidel, näitasid luumurdude riski suurenemist patsientidel, kellele manustati SSRI -sid ja TCA -sid. Selle suurenenud riski taga olev mehhanism on teadmata.
Pärast ravi lõpetamist fluoksetiiniga täheldati võõrutusnähte
Fluoksetiinravi katkestamine põhjustab tavaliselt võõrutusnähte.
Pearinglus, sensoorsed häired (sh paresteesia), unehäired (sh unetus ja intensiivsed unenäod), asteenia, erutus või ärevus, iiveldus ja / või oksendamine, värin ja peavalu on kõige sagedamini teatatud reaktsioonid.
Üldiselt on need sündmused kerged / mõõdukad ja iseenesest mööduvad, kuid mõnedel patsientidel võivad need olla rasked ja / või pikaajalised (vt lõik "Ettevaatusabinõud kasutamisel"). Seetõttu on soovitatav, kui ravi Fluoxeren’iga ei ole enam vajalik järkjärguline ärajätmine, vähendades annust (vt "Annus, manustamisviis ja aeg" ja "Ettevaatusabinõud kasutamisel").
Lapsed (vt lõigud "Ettevaatusabinõud kasutamisel")
Laste kliinilistes uuringutes olid enesetapuga seotud käitumised (enesetapukatse ja enesetapumõtted), vaenulikkus (teatatud sündmused olid: viha, ärrituvus, agressiivsus, erutus, hüperaktiivsuse sündroom), maniakaalsed reaktsioonid, sealhulgas maania ja hüpomaania (ilma nendel patsientidel varem teatatud episoodidena) ) ja ninaverejooksu tekkisid sageli ja neid täheldati sagedamini antidepressantidega ravitud laste ja noorukite seas kui platseebot saanud patsientidel.
Fluoksetiini ohutust kroonilise ravi korral ei ole süstemaatiliselt hinnatud üle 19 nädala.
Laste kliinilistes uuringutes on teatatud maniakaalsetest reaktsioonidest, sealhulgas maaniast ja hüpomaaniast (2,6% fluoksetiiniga ravitud patsientidest vs 0% platseebokontrolliga patsientidest), mis on enamikul juhtudel lõpetanud ravi. Nendel patsientidel ei olnud esinenud esimesi hüpomaania episoode. maania.
Pärast 19 -nädalast ravi teatasid kliinilises uuringus fluoksetiiniga ravitud lastel keskmiselt 1,1 cm vähem (p = 0,004) ja 1,1 kg vähem (p = 0,008) kui platseebot saanud patsientidel.
Kliinilise kasutamise ajal on teatatud ka üksikutest kasvupeetuse juhtudest.
Laste populatsioonis läbi viidud kliinilistes uuringutes seostati fluoksetiinravi leeliselise fosfataasi taseme langusega.
Laste kliinilises kasutamises on teatatud üksikutest kõrvaltoimetest, mis võivad viidata seksuaalse küpsemise hilinemisele või seksuaalsele düsfunktsioonile.
Arvatavatest kõrvaltoimetest teatamine
Pärast ravimi müügiloa väljastamist tekkinud arvatavatest kõrvaltoimetest teatamine on oluline, kuna see võimaldab pidevalt jälgida ravimi kasu ja riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest riikliku teavitussüsteemi kaudu. "Aadress www. agenziafarmaco.gov.it/it/responsabili
Aegumine ja säilitamine
Aegumine: vaadake pakendil märgitud aegumiskuupäeva.
Kõlblikkusaeg viitab puutumata pakendis olevale tootele, mis on õigesti hoitud.
ETTEVAATUST: Ärge kasutage ravimit pärast pakendil märgitud kõlblikkusaja lõppu.
FLUOXEREN 20 mg kõvakapslid ja FLUOXEREN 20 mg / 5 ml suukaudne lahus
Hoida temperatuuril kuni 25 ° C.
FLUOXEREN 20 mg dispergeeruvad tabletid
Hoida temperatuuril kuni 30 ° C.
Ravimeid ei tohi ära visata kanalisatsiooni kaudu ega koos majapidamisprügiga. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
HOIDA RAVIMPREPARAADI LASTE EEST KÄTTESAAMATUS KOHAS
Tähtaeg "> Muu teave
KOOSTIS
FLUOXEREN 20 mg kõvakapslid
Iga kõvakapsel sisaldab:
- toimeaine: fluoksetiinvesinikkloriid 22,36 mg, mis vastab 20,00 mg fluoksetiinile
- abiained: maisitärklis, dimetikoon, lakitud sinine V E-131, kollane raudoksiid E-172, titaandioksiid E-171, želatiin
FLUOXEREN 20 mg / 5 ml suukaudne lahus
5 ml suukaudset lahust sisaldab:
- toimeaine: fluoksetiinvesinikkloriid 22,36 mg, mis vastab 20,00 mg fluoksetiinile
- Abiained: bensoehape, sahharoos, glütseriin, piparmündimaitse, puhastatud vesi
FLUOXEREN 20 mg dispergeeruvad tabletid
Iga dispergeeruv tablett sisaldab:
- toimeaine: fluoksetiinvesinikkloriid 22,36 mg, mis vastab 20,00 mg fluoksetiinile
- Abiained: mikrokristalne tselluloos, naatriumsahhariin, mannitool, sorbitool, aniisi maitseaine, piparmündi lõhna- ja maitseaine, veevaba kolloidne ränidioksiid, eelgeelistatud tärklis, naatriumstearüülfumaraat, krospovidoon
RAVIMVORM JA SISU
- 12 ja 28 kõvakapslit, igaüks 20 mg
- 60 ml 20 mg / 5 ml suukaudset lahust
- 12 ja 28 dispergeeruvat tabletti, igaüks 20 mg
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS -
FLUOXEREN
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS -
FLUOXEREN 20 mg kõvakapslid
Iga kõvakapsel sisaldab:
aktiivne põhimõte: 22,36 mg fluoksetiinvesinikkloriidi, mis vastab 20,00 mg fluoksetiinile.
FLUOXEREN 20 mg / 5 ml suukaudne lahus
5 ml suukaudset lahust sisaldab:
aktiivne põhimõte: 22,36 mg fluoksetiinvesinikkloriidi, mis vastab 20,00 mg fluoksetiinile.
FLUOXEREN 20 mg dispergeeruvad tabletid
Iga dispergeeruv tablett sisaldab:
aktiivne põhimõte: 22,36 mg fluoksetiinvesinikkloriidi, mis vastab 20,00 mg fluoksetiinile.
Abiainete täielik loetelu vt lõik 6.1.
03.0 RAVIMVORM -
Kõvakapsel, dispergeeruv tablett, suukaudne lahus.
04.0 KLIINILINE TEAVE -
04.1 Näidustused -
Peamised depressiooni episoodid.
Obsessiiv-kompulsiivne häire.
Bulimia nervosa: Fluoxeren on näidustatud koos psühhoteraapiaga, et vähendada liigsöömist ja puhastamist.
04.2 Annustamine ja manustamisviis
Suukaudseks manustamiseks.
Peamised depressiooni episoodid
Täiskasvanud ja eakad: soovitatav annus on 20 mg ööpäevas. Vajadusel tuleb annus üle vaadata ja kohandada 3-4 nädala jooksul pärast ravi alustamist ja seejärel kliiniliselt sobivaks peetuna. Kuigi suuremate annuste korral võib kõrvaltoimete tekkerisk suureneda mõnel ebapiisava ravivastusega patsiendil. mg, võib annust järk -järgult suurendada kuni maksimaalse 60 mg -ni (vt lõik 5.1). Annust tuleb kohandada iga patsiendi puhul ettevaatlikult, et hoida patsiente väikseima efektiivse annusega.
Depressiooniga patsiente tuleb ravida piisavalt kaua, vähemalt 6 kuud, et olla kindel, et neil pole sümptomeid.
Obsessiiv-kompulsiivne häire
Täiskasvanud ja eakad: soovitatav annus on 20 mg ööpäevas. Kuigi suuremate annuste korral võib kõrvaltoimete oht suureneda, võib mõnedel patsientidel annust suurendada kuni 60 mg -ni, kui pärast 2 -nädalast ravi 20 mg -ga ei saavutata piisavat ravivastust.
Kui 10 nädala jooksul paranemist ei täheldata, tuleb fluoksetiinravi uuesti kaaluda. Kui on saavutatud hea ravivastus, võib ravi jätkata, kohandades annust individuaalselt. Kuigi süstemaatilisi uuringuid fluoksetiinravi jätkamise aja määramiseks ei ole läbi viidud, on OCD krooniline haigus ja ravile alluvatel patsientidel on mõistlik kaaluda ravi pikendamist üle 10 nädala. Annust tuleb muuta iga patsiendi puhul ettevaatlikult, et hoida patsienti väikseima efektiivse annusena. Ravi vajadust tuleb perioodiliselt uuesti hinnata. Mõned arstid peavad samaaegset käitumuslikku psühhoteraapiat kasulikuks patsientidele, kes on ravile hästi reageerinud. Obsessiiv-kompulsiivse häire korral ei ole pikaajalist (üle 24 nädala) efektiivsust tõestatud.
Buliimia
Täiskasvanud ja eakad: soovitatav annus on 60 mg ööpäevas. Pikaajalist (üle 3 kuu) efektiivsust ei ole tõestatud bulimia nervosa korral.
Täiskasvanud - kõik näidustused
Soovitatavat annust võib suurendada või vähendada. Üle 80 mg ööpäevaseid annuseid ei ole süstemaatiliselt hinnatud.
Fluoksetiini võib manustada ühe või mitme annusena, koos toiduga või ilma.
Kui annustamine lõpetatakse, püsivad farmakoloogiliselt aktiivsed ained kehas nädalaid, mida tuleb ravi alustamisel või lõpetamisel arvesse võtta.
Kapsel ja vedelad vormid on bioekvivalentsed.
8 -aastased ja vanemad lapsed ja noorukid (mõõdukas kuni raske raske depressiooni episood)
Ravi tuleb alustada ja jälgida spetsialisti järelevalve all. Algannus on 10 mg päevas, manustatuna 2,5 ml Fluoxereni suukaudse lahusena. Annust tuleb kohandada ettevaatlikult ja individuaalselt, et hoida patsient väikseima efektiivse annusena.
1-2 nädala pärast võib annust suurendada 20 mg -ni päevas. Kliiniline kogemus üle 20 mg ööpäevaste annuste kasutamisel on minimaalne. Üle 9 nädala kestnud ravi kohta on andmed piiratud.
Madala kehakaaluga lapsed
Kuna vähenenud kehakaaluga lastel on plasmakontsentratsioon kõrgem, saab ravitoime saavutada väiksemate annustega (vt lõik 5.2).
Ravile alluvate pediaatriliste patsientide puhul tuleb uuesti hinnata vajadust jätkata ravi 6 kuu pärast. Kui 9 nädala jooksul ei saavutata kliinilist kasu, tuleb ravi uuesti läbi vaadata.
Eakad kodanikud
Annuse suurendamisel on soovitatav olla ettevaatlik ja üldiselt ei tohi päevane annus ületada 40 mg. Maksimaalne soovitatav annus on 60 mg päevas.
Maksapuudulikkusega patsientidel (vt lõik 5.2) või patsientidel, kellel on võimalik koostoime Fluoxereni ja samaaegse kasutamise vahel, tuleb kaaluda väiksema või harvema annuse (nt 20 mg igal teisel päeval) manustamist (vt lõik 5.2). lõik 4.5).
Pärast Fluoxeren -ravi lõpetamist täheldati võõrutusnähte
Ravi järsku katkestamist tuleb vältida. Fluoxeren -ravi katkestamisel tuleb annust järk -järgult vähendada vähemalt 1 ... 2 nädala jooksul, et vähendada võõrutusreaktsioonide riski (vt lõigud 4.4 ja 4.8).
Kui pärast annuse vähendamist või ravi katkestamist tekivad talumatud sümptomid, võib kaaluda varem määratud annuse jätkamist. Seejärel võib arst jätkata annuse vähendamist, kuid järk -järgult.
04.3 Vastunäidustused -
Ülitundlikkus toimeaine või lõigus 6.1 loetletud mis tahes abiainete suhtes.
Fluoksetiin on vastunäidustatud koos:
- pöördumatud ja mitteselektiivsed monoamiini oksüdaasi inhibiitorid (nt iproniasiid) (vt lõigud 4.4 ja 4.5);
- südamepuudulikkuse korral kasutatav metoprolool (vt lõik 4.5).
04.4 Erihoiatused ja ettevaatusabinõud kasutamisel -
Lapsed - alla 18 -aastased lapsed ja noorukid
Kliinilistes uuringutes täheldati antidepressantidega ravitud lastel ja noorukitel sagedamini suitsiidiga seotud käitumist (enesetapukatseid ja enesetapumõtteid) ja vaenulikkust (peamiselt agressiivsust, vastandlikku käitumist ja viha) kui platseebot saanud patsientidel. Fluoxeren on ette nähtud kasutamiseks lastel ja noorukitel vanuses 8 kuni 18 aastat mõõduka kuni raske depressiooni episoodide raviks ning seda ei tohi kasutada muude näidustuste korral. Kui meditsiiniliste vajaduste põhjal otsustatakse ravi üle, tuleb patsienti hoolikalt jälgida enesetapumõjude ilmnemise suhtes. Lisaks on laste ja noorukite kohta saadaval ainult piiratud pikaajalised ohutusandmed, sealhulgas mõju kasvule, seksuaalsele küpsemisele ning kognitiivsele, emotsionaalsele ja käitumuslikule arengule (vt lõik 5.3).
19-nädalases kliinilises uuringus täheldati fluoksetiiniga ravitud lastel ja noorukitel nii pikkuse kui ka kehakaalu vähenemist (vt lõik 5.1). Ei ole kindlaks tehtud, kas sellel on mõju täiskasvanueas normaalse pikkuse saavutamisele. hilinenud puberteeti ei saa välistada (vt lõigud 5.3 ja 4.8). Seetõttu tuleb fluoksetiinravi ajal ja pärast seda jälgida puberteedi kasvu ja arengut (pikkus, kaal ja TANNERi staadium). aeglustunud, tuleb kaaluda pediaatrilist konsultatsiooni .
Lastel läbi viidud uuringutes teatati sageli maaniast ja hüpomaaniast (vt lõik 4.8). Seetõttu on soovitatav regulaarselt jälgida maania / hüpomaania esinemist. Maniakaalsesse faasi siseneva patsiendi puhul tuleb fluoksetiinravi katkestada.
On oluline, et arst arutaks hoolikalt lapsega / noorukiga ja / või tema vanematega ravi riske ja kasu.
Nahalööve ja allergilised reaktsioonid
On teatatud lööbest, anafülaktoidsetest sündmustest ja progresseeruvatest süsteemsetest sündmustest, mõnikord tõsistest (naha, neerude, maksa või kopsude puhul). Nahalööbe või muude allergiliste nähtude korral, mille puhul ei ole võimalik kindlaks teha erinevat etioloogiat, tuleb fluoksetiini manustamine katkestada.
Krambid
Krambid kujutavad endast potentsiaalset riski antidepressantide kasutamisel. Seetõttu, nagu ka teiste antidepressantide puhul, tuleb fluoksetiini manustada ettevaatusega patsientidele, kellel on esinenud krampe. Ravi tuleb katkestada kõigil patsientidel, kellel esinevad krambid või kellel on täheldatud krampide esinemissageduse suurenemist. Ebastabiilsete krambihoogude / epilepsiaga patsientidel tuleb fluoksetiini manustamist vältida ja kontrollitud epilepsiaga patsiente tuleb hoolikalt jälgida (vt lõik 4.5).
Elektrokonvulsioonravi (TEC)
TEC-ravi saavatel fluoksetiiniga ravitud patsientidel on harvadel juhtudel teatatud pikaajalistest krampidest, seetõttu on soovitatav olla ettevaatlik.
Mania
Antidepressante tuleb mania / hüpomaania anamneesiga patsientidel kasutada ettevaatusega. Nagu kõigi antidepressantide puhul, tuleb fluoksetiinravi katkestada kõigil maniakaalses faasis olevatel patsientidel.
Maksa / neerufunktsioon
Fluoksetiin metaboliseerub ulatuslikult maksas ja eritub neerude kaudu. Märkimisväärse maksafunktsiooni häirega patsientidel on soovitatav kasutada väiksemat annust, nt manustada igal teisel päeval. Kui fluoksetiini manustati 2 kuu jooksul annustes 20 mg ööpäevas, olid raske neerukahjustusega patsiendid (GFR dialüüs ei näidanud erinevusi fluoksetiini ega norfluoksetiini plasmatasemes võrreldes normaalse neerufunktsiooniga kontrollrühmaga).
Tamoksifeen
Fluoksetiin, mis on tugev CYP2D6 inhibiitor, võib vähendada endoksifeeni, mis on üks olulisemaid tamoksifeeni aktiivseid metaboliite, kontsentratsiooni. Seetõttu tuleb tamoksifeenravi ajal vältida fluoksetiini manustamist võimaluse korral (vt lõik 4.5).
Kardiovaskulaarsed mõjud
312 patsiendil, kes said topeltpimedates kliinilistes uuringutes fluoksetiini, ei täheldatud elektrokardiogrammis juhtivushäireid, mis põhjustasid südame seiskumist, kuid ägeda südamehaiguse kliiniline kogemus on piiratud, seetõttu on soovitatav olla ettevaatlik. Turuletulekujärgsel perioodil on teatatud QT-intervalli pikenemise ja ventrikulaarse arütmia juhtudest, sealhulgas torsade de pointes (vt lõigud 4.5, 4.8 ja 4.9).
Fluoksetiini tuleb kasutada ettevaatusega patsientidel, kellel on sellised haigused nagu kaasasündinud pika QT sündroom, QT -intervalli pikenemine perekonnas või muud arütmiale eelsoodumusega kliinilised seisundid (nt hüpokaleemia, hüpomagneseemia, bradükardia, äge müokardiinfarkt või dekompenseeritud südamepuudulikkus). fluoksetiin (nt maksapuudulikkus).
Kui ravitakse stabiilse südamehaigusega patsiente, tuleb enne ravi alustamist kaaluda EKG -d.
Kui fluoksetiinravi ajal ilmnevad südame rütmihäire nähud, tuleb ravi katkestada ja teha EKG.
Kaalukaotus
Fluoksetiini võtvatel patsientidel võib tekkida kehakaalu langus, kuid see on tavaliselt proportsionaalne algkaaluga.
Diabeet
Diabeediga patsientidel võib SSRI -ravi muuta glükeemilist kontrolli. Hüpoglükeemia tekkis fluoksetiinravi ajal, samas kui hüperglükeemia tekkis pärast ravimi kasutamise lõpetamist. Vajalikuks võib osutuda insuliini ja / või suukaudse hüpoglükeemilise aine annuse kohandamine.
Enesetapp / enesetapumõtted või kliiniline halvenemine
Depressioon on seotud enesetapumõtete, enesevigastamise ja enesetapu (suitsiidiga seotud sündmused) suurenenud riskiga. See oht püsib kuni haiguse märkimisväärse remissioonini. Kuna paranemine ei pruugi ilmneda ravi esimestel nädalatel või kauem, tuleb patsiente tähelepanelikult jälgida kuni paranemiseni. On tavaline kliiniline kogemus, et enesetapurisk võib paranemisprotsessi alguses suureneda.
Teised psühhiaatrilised seisundid, mille puhul Fluoxeren on ette nähtud, võivad samuti olla seotud suitsiidikäitumise suurenenud riskiga. Lisaks võib neid seisundeid seostada raske depressiivse häirega. Järelikult tuleb järgida samu ettevaatusabinõusid, mida järgitakse raske depressiooniga patsientide ravimisel ka teiste psühhiaatriliste häiretega patsientide ravimisel.
Patsientidel, kellel on anamneesis suitsiidiga seotud sündmusi või kellel esineb enne ravi alustamist märkimisväärne enesetapumõte, on suurem risk enesetapumõteteks või enesetapukatseks ning neid tuleb ravi ajal hoolikalt jälgida. Platseeboga kontrollitud kliinilised uuringud psühhiaatriliste häiretega täiskasvanud patsientidel, kes saavad antidepressante, on näidatud suurenenud suitsidaalse käitumise riski alla 25 -aastastel patsientidel, kes said antidepressante, võrreldes platseeboga ravitud patsientidega.
Ravi ajal, eriti ravi alguses ja pärast annuse muutmist, on vajalik patsientide, eriti kõrge riskiga patsientide hoolikas jälgimine. Patsiente (ja nende hooldajaid) tuleb teavitada vajadusest kontrollida kliinilist halvenemist, enesetapumõjude ilmnemist. käitumist või mõtteid ning ebatavalisi muutusi käitumises ja nende sümptomite ilmnemisel pöörduge viivitamatult arsti poole.
Akatisia / psühhomotoorne rahutus
Fluoksetiini kasutamist on seostatud akatiisia tekkimisega, mida iseloomustab subjektiivselt ebameeldiv või valulik rahutustunne ja psühhomotoorne erutus, millega kaasneb võimetus paigal istuda või seista. See juhtub kõige tõenäolisemalt ravi esimestel nädalatel. Nende sümptomitega patsientidel võib annuse suurendamine olla kahjulik.
Pärast SSRI -ravi lõpetamist täheldati võõrutusnähte
Ravi katkestamise sümptomid on sagedased, eriti järsu katkestamise korral (vt lõik 4.8).
Kliinilistes uuringutes esines ravi katkestamisel täheldatud kõrvaltoimeid 60% -l patsientidest nii fluoksetiini kui ka platseebo rühmas. Nendest kõrvaltoimetest olid 17% fluoksetiinirühmas ja 12% fluoksetiinigrupis platseebost rasked.
Võõrutusnähtude risk võib sõltuda mitmest tegurist, sealhulgas ravi kestusest, annusest ja annuse vähendamise kiirusest.
Kõige sagedamini teatatud reaktsioonid on pearinglus, sensoorsed häired (sh paresteesia), unehäired (sh unetus ja intensiivsed unenäod), asteenia, erutus või ärevus, iiveldus ja / või oksendamine, värisemine ja peavalu. Üldiselt on nende sümptomite intensiivsus kerge kuni mõõdukas, kuid mõnel patsiendil võivad need olla rasked. Need ilmnevad tavaliselt esimestel päevadel pärast ravi lõpetamist. Üldiselt on need sümptomid iseenesest mööduvad ja kaovad tavaliselt kahe päeva jooksul. kuigi mõnedel inimestel võivad need kesta kauem (2-3 kuud või kauem). Seetõttu on soovitatav ravi lõpetamisel Fluoxeren'i annust järk-järgult vähendada, vähemalt 1 ... 2 nädala jooksul, sõltuvalt patsiendi vajadustest (vt punkt 4.2, Fluoxeren -ravi lõpetamisel täheldati võõrutusnähte).
Verejooks
SSRI -de kasutamisel on teatatud nahaverejooksu ilmingutest, nagu ekhümoos ja purpur.Fluoksetiinravi ajal on harva esinenud ekhümoosi. Harva on teatatud muudest hemorraagilistest ilmingutest (nt günekoloogilised verejooksud, seedetrakti verejooks ja muu naha- või limaskestaverejooks). SSRI -sid kasutavatel patsientidel on soovitatav olla ettevaatlik, eriti samaaegsel kasutamisel. suukaudsed antikoagulandid, trombotsüütide funktsiooni mõjutavad ravimid või muud ravimid, mis võivad suurendada verejooksu riski (nt ebatüüpilised antipsühhootikumid, nagu klosapiin, fenotiasiinid, enamik tritsüklilistest antidepressantidest, aspiriin, MSPVA -d, samuti patsientidel, kellel on anamneesis patoloogilistest ilmingutest, mida iseloomustab verejooks (vt lõik 4.5).
Müdriaas
Fluoksetiiniga seoses on teatatud müdriaasist; Seetõttu tuleb olla ettevaatlik fluoksetiini määramisel kõrgendatud silmasisese rõhuga või ägeda kitsanurga glaukoomi riskiga patsientidele.
Naistepuna
Kui selektiivsed serotoniini tagasihaarde inhibiitorid ja naistepuna sisaldavad taimsed preparaadid (Hypericum perforatum) kasutatakse koos, võib esineda suurenenud serotoniinergilist toimet, näiteks serotoniinisündroom.
Serotoniini sündroom või pahaloomulise neuroleptilise sündroomi sarnased sündmused
Harvadel juhtudel on seoses fluoksetiinraviga teatatud serotoniinisündroomi või pahaloomulise neuroleptilise sündroomi sarnaste sündmuste tekkest, eriti kui fluoksetiini manustatakse koos teiste serotoniinergiliste ravimitega (muuhulgas L-trüptofaan) ja / või neuroleptikumidega (vt lõik 4.5). Kuna need sündroomid võivad tekitada patsiendile potentsiaalselt eluohtlikke seisundeid, võivad selliste nähtude ilmnemisel tekkida (neid iseloomustavad mitmed sümptomid nagu hüpertermia, jäikus, müokloonus, autonoomse närvisüsteemi ebastabiilsus koos võimalike kiirete elutähtsate kõikumistega, vaimne seisund, sealhulgas segasus, ärrituvus ja äärmine erutus kuni deliiriumi ja koomani), tuleb fluoksetiinravi katkestada ja alustada sümptomaatilist toetavat ravi.
Pöördumatud mitteselektiivsed monoamiini oksüdaasi inhibiitorid (nt iproniasiid)
On teatatud tõsistest ja mõnikord surmavatest reaktsioonidest patsientidel, kes kasutasid SSRI-d koos pöördumatu mitteselektiivse monoamiini oksüdaasi inhibiitoriga (MAOI).
Nendel juhtudel on serotoniinisündroomiga sarnased tunnused (ja neid võib segi ajada (või diagnoosida) pahaloomulise neuroleptilise sündroomiga). Tsüproheptadiinist või dantroleenist võib selliste reaktsioonidega patsientidele kasu olla. Ravimi koostoime sümptomid MAOI -ga on järgmised: hüpertermia, jäikus, müokloonus, autonoomne ebastabiilsus koos võimalike kiirete elutähtsate kõikumistega, vaimse seisundi muutused, sealhulgas segasus, ärrituvus ja äärmine erutus kuni deliiriumi ja koomani.
Seetõttu on fluoksetiin vastunäidustatud kombinatsioonis pöördumatu mitteselektiivse MAOI-ga (vt lõik 4.3). Kuna viimase toime kestab 2 nädalat, tuleb fluoksetiinravi alustada alles 2 nädalat pärast pöördumatu mitteselektiivse MAOI lõpetamist. Samamoodi peaks enne fluoksetiinravi katkestamist mööduma vähemalt 5 nädalat enne ravi alustamist pöördumatu mitteselektiivse selektiivne MAOI.
Oluline teave mõne koostisosa kohta
FLUOXEREN 20 mg / 5 ml suukaudne lahus sisaldab sahharoosi. Patsiendid, kellel on harvaesinev pärilik fruktoositalumatus, glükoosi imendumishäire või sahharaasi isomaltaasi puudulikkus, ei tohi seda ravimit võtta.
FLUOXEREN 20 mg dispergeeruvad tabletid sisaldavad sorbitooli. Patsiendid, kellel on harvaesinev pärilik fruktoositalumatus, ei tohi seda ravimit võtta.
04.5 Koostoimed teiste ravimitega ja muud koostoimed -
Koostoimeuuringuid on läbi viidud ainult täiskasvanutel.
Pool elu: Kui arvestada farmakodünaamilisi või farmakokineetilisi koostoimeid (nt fluoksetiinilt teistele antidepressantidele üleminekul), tuleb arvestada nii fluoksetiini kui ka norfluoksetiini pika eliminatsiooni poolväärtusajaga (vt lõik 5.2).
Vastunäidustatud ühendused
Pöördumatud mitteselektiivsed monoamiini oksüdaasi inhibiitorid (nt ipronasiid)
On teatatud tõsistest ja mõnikord surmavatest reaktsioonidest patsientidel, kes kasutasid SSRI-d koos pöördumatu mitteselektiivse monoamiini oksüdaasi inhibiitoriga (MAOI).
Nendel juhtudel on serotoniinisündroomiga sarnased tunnused (ja neid võib segi ajada (või diagnoosida) pahaloomulise neuroleptilise sündroomiga).
Tsüproheptadiinist või dantroleenist võib selliste reaktsioonidega patsientidele kasu olla. Ravimi koostoime sümptomid MAOI -ga on järgmised: hüpertermia, jäikus, müokloonus, autonoomne ebastabiilsus koos võimalike kiirete elutähtsate kõikumistega, vaimse seisundi muutused, sealhulgas segasus, ärrituvus ja äärmine erutus kuni deliiriumi ja koomani.
Seetõttu on fluoksetiin vastunäidustatud kombinatsioonis pöördumatu mitteselektiivse MAOI-ga (vt lõik 4.3). Kuna viimase toime kestab 2 nädalat, tuleb fluoksetiinravi alustada alles 2 nädalat pärast pöördumatu mitteselektiivse MAOI lõpetamist. Samamoodi peaks enne fluoksetiinravi katkestamist mööduma vähemalt 5 nädalat enne ravi alustamist pöördumatu mitteselektiivse selektiivne MAOI.
Südamepuudulikkuse korral kasutatav metoprolool: Metoprolooli kõrvaltoimete, sealhulgas liigse bradükardia risk võib suureneda selle metabolismi pärssimise tõttu fluoksetiini poolt (vt lõik 4.3).
Kombinatsioone ei soovitata
TamoksifeenKirjanduses on kirjeldatud farmakokineetilist koostoimet CYP2D6 inhibiitorite ja tamoksifeeni vahel, kusjuures ühe kõige aktiivsema tamoksifeenivormi ehk endoksifeeni plasmakontsentratsioon väheneb 65-75%. Mõnedes uuringutes on teatatud tamoksifeeni efektiivsuse vähenemisest, mida manustatakse samaaegselt mõne SSRI antidepressandiga. Kuna seda tamoksifeeni toime vähenemist ei saa välistada, tuleks võimalusel vältida tugevate CYP2D6 inhibiitorite (sh fluoksetiini) samaaegset manustamist (vt. lõik 4.4).
Alkohol: Rutiinsetes testides ei põhjusta fluoksetiin vere alkoholisisalduse tõusu ega võimenda alkoholi toimet, kuid SSRI ja alkoholravi kombinatsioon ei ole soovitatav.
MAOI-tüüp A, sealhulgas linezolid ja metüültioniiniumkloriid (metüleensinine): serotoniinisündroomi, sealhulgas kõhulahtisuse, tahhükardia, higistamise, värisemise, segasuse või kooma oht. Kui nende toimeainete samaaegset kasutamist koos fluoksetiiniga ei saa vältida, tuleb hoolikalt jälgida kliinilist seisundit ja alustada samaaegsete ravimite manustamist võimalikult väikeste soovitatud annustega (vt lõik 4.4).
Mekitasiin: võib esineda suurenenud risk kõrvaltoimete tekkeks (nt QT -intervalli pikenemine), mis on tingitud selle metabolismi pärssimisest fluoksetiini poolt.
Ettevaatust nõudvad ühendused
Fenitoiina: Fluoksetiiniga kombineerituna on täheldatud muutusi veres. Mõnel juhul on esinenud toksilisuse ilminguid. Seetõttu on soovitatav manustada samaaegselt kasutatavat ravimit vastavalt konservatiivsetele raviskeemidele ja hoolikalt jälgida patsiendi kliinilisi seisundeid.
Serotoniinergilised ravimid [liitium, tramadool, triptaanid, trüptofaan, selegiliin (MAOI-tüüp B), naistepuna (Hypericum perforatum)]: Pärast SSRI -de manustamist koos ravimitega, millel on ka serotonergiline toime, on teatatud mõõduka serotoniinisündroomi tekkest. Seetõttu tuleb fluoksetiini samaaegselt kasutada nende ravimitega ettevaatlikult, sihipärasema kliinilise jälgimisega ja sagedamini (vt. lõik 4.4).
Seos triptaanidega lisab täiendavat riski pärgarterite vasokonstriktsiooni ja hüpertensiooni tekkeks.
QT -intervalli pikenemineFarmakokineetilisi ja farmakodünaamilisi uuringuid fluoksetiini ja teiste QT -intervalli pikendavate ravimite kombinatsiooni kohta ei ole läbi viidud. Ei saa välistada fluoksetiini ja nende ravimite aditiivset toimet. Seetõttu on fluoksetiini ja QT -intervalli pikendavate ravimite - nagu IA ja III klassi antiarütmikumid, antipsühhootikumid (nt fenotiasiini derivaadid, pimosiid, haloperidool), tritsüklilised antidepressandid, mõned antimikroobsed ained (nt sparfloksatsiin, moksifloksatsiin), erütromütsiin - samaaegne manustamine , malaariavastane ravi, eriti halofantriin, mõned antihistamiinikumid (astemisool, misolastiin) - nõuab ettevaatust (vt lõigud 4.4, 4.8 ja 4.9).
Hemostaasi mõjutavad ravimid (suukaudsed antikoagulandid, olenemata nende toimemehhanismist, trombotsüütidevastased ained, sh aspiriin ja MSPVA -d): suurenenud verejooksu oht. Kliiniline jälgimine ja sagedasem INR -i jälgimine tuleb läbi viia suukaudsete antikoagulantidega. Annuse kohandamine võib osutuda vajalikuks fluoksetiinravi ajal ja pärast ravi lõpetamist (vt lõigud 4.4 ja 4.8).
Küprosheptadiin: Üksikutel juhtudel on teatatud fluoksetiini antidepressantide aktiivsuse vähenemisest, kui seda kasutatakse koos tsüproheptadiiniga.
Hüponatreemiat esile kutsuvad ravimid: Hüponatreemia on fluoksetiini soovimatu toime.Kasutamine koos teiste hüponatreemiaga seotud ainetega (nt diureetikumid, desmopressiin, karbamasepiin ja okskarbasepiin) võib suurendada riski (vt lõik 4.8).
Ravimid, mis alandavad epileptogeenset läve: Krambid on fluoksetiini soovimatu toime. Riski võib suurendada, kui seda kasutatakse koos teiste epileptogeenset läve alandavate ainetega (nt TCA, teised SSRI -d, fenotiasiinid, butürofenoonid, meflokviin, klorokiin, buproprioon, tramadool).
Muud ravimid, mida metaboliseerib CYP2D6: fluoksetiin on tugev ensüümi CYP2D6 inhibiitor, seetõttu võib samaaegne ravi ravimitega, mida samuti see ensüümsüsteem metaboliseerib, põhjustada ravimite koostoimeid, eriti kui on tegemist kitsa terapeutilise indeksiga ravimitega (nt flekainiid, enkainiid, propafenoon ja nebivolool) ja tiitritud ravimeid, aga ka atomoksetiini, karbamasepiini, tritsükliliste antidepressantide ja risperidooni. Nende manustamist tuleb alustada või kohandada alates annuste vahemiku madalaimast väärtusest. Seda tuleks teha ka siis, kui eelneva 5 nädala jooksul on olnud fluoksetiini.
04.6 Rasedus ja imetamine -
Rasedus
Mõned epidemioloogilised uuringud näitavad fluoksetiini kasutamisega seotud esimesel kardiovaskulaarsel perioodil suurenenud kardiovaskulaarsete defektide riski. Mehhanism on teadmata. Üldiselt näitavad andmed, et pärast emade fluoksetiiniga kokkupuudet on vastsündinu risk kardiovaskulaarse häirega 2 /100 võrreldes selliste defektide eeldatava määraga umbes 1/100 üldpopulatsioonis.
Epidemioloogilised andmed on näidanud, et SSRI -de kasutamine raseduse ajal, eriti raseduse lõpus, võib suurendada vastsündinu püsiva pulmonaalse hüpertensiooni (PPHN) riski. Täheldatud risk oli ligikaudu 5 rasedust 1000 -st. Üldpopulatsioonis kuni 2 PPHN juhtu 1000 raseduse kohta.
Lisaks, kuigi fluoksetiini võib raseduse ajal kasutada, tuleb olla ettevaatlik, eriti raseduse hilises staadiumis või vahetult enne sünnituse algust, sest vastsündinutel on teatatud järgmistest toimetest: ärrituvus, värisemine, hüpotoonia, püsiv nutt, imemis- või magamisraskused. Need sümptomid võivad viidata nii serotonergilisele toimele kui ka võõrutussündroomile. Nende sümptomite ilmnemise aeg ja kestus võivad olla seotud fluoksetiini ja selle aktiivse metaboliidi norfluoksetiini pika poolväärtusajaga (4-6 päeva). (4-16 päeva).
Toitmisaeg
On teada, et fluoksetiin ja selle aktiivne metaboliit norfluoksetiin erituvad inimese rinnapiima. Imetavatel imikutel on teatatud kõrvaltoimetest. Kui ravi fluoksetiiniga peetakse vajalikuks, tuleb kaaluda rinnaga toitmise katkestamist, kuid kui rinnaga toitmist jätkatakse, tuleb määrata madalaim efektiivne fluoksetiini annus.
Viljakus
Loomkatsed on näidanud, et fluoksetiin võib mõjutada sperma kvaliteeti (vt lõik 5.3). Inimeste juhtumite aruanded mõnede SSRI -dega on näidanud, et mõju sperma kvaliteedile on pöörduv. Mõju inimese viljakusele ei ole seni täheldatud.
04.7 Toime autojuhtimise ja masinate käsitsemise võimele -
Fluoxeren ei mõjuta või mõjutab ebaoluliselt autojuhtimise ja masinate käsitsemise võimet. Kuigi on tõestatud, et fluoksetiin ei häiri tervetel vabatahtlikel psühhomotoorseid oskusi, võib iga psühhoaktiivne ravim kahjustada otsustusvõimet või psühhomotoorseid oskusi. Patsiente tuleb soovitada vältida sõiduki juhtimist või ohtlike masinatega töötamist, kuni nad on piisavalt kindlad, et nende võimed ei ole halvenenud.
04.8 Kõrvaltoimed -
kuni) Ohutusprofiili kokkuvõte
Kõige sagedamini teatatud kõrvaltoimed fluoksetiiniga ravitud patsientidel olid peavalu, iiveldus, unetus, väsimus ja kõhulahtisus. Kõrvaltoimete intensiivsus ja esinemissagedus võivad ravi jätkudes väheneda ega vaja tavaliselt ravi katkestamist.
b) Kõrvaltoimete tabel
Allolevas tabelis on toodud kõrvaltoimed, mida täheldati fluoksetiinravi ajal täiskasvanutel ja lastel. Mõned neist kõrvaltoimetest on tavalised ka teiste SSRI -de puhul.
Allpool esitatud sagedused arvutati täiskasvanute kliiniliste uuringute (n = 9297) ja spontaansete aruannete põhjal.
Hinnanguline esinemissagedus: väga sage (≥ 1/10); sage (≥ 1/100 kuni
¹ Kaasa arvatud anoreksia
² Sisaldab varajast ärkamist hommikul, esmast unetust, vahepealset unetust
³ Sisaldab libiido kaotust
4 Sisaldab õudusunenägusid
5 Sisaldab anorgasmiat
6 Hõlmab lõpetatud enesetappu, enesetapumõtet, tahtlikku enesevigastamist, enesevigastamist, enesetapukäitumist, enesetapumõtteid, enesetapukatse, haigeid mõtteid, enesevigastamist. Need sümptomid võivad olla põhjustatud haigusest.
7 Kaasa arvatud hüpersomnia, sedatsioon
8 Sisaldab kuumahooge
9 Hõlmab atelektaasi, interstitsiaalset kopsuhaigust, kopsupõletikku
10 Kõige sagedamini hõlmab igemete verejooksu, hematemeesi, hematokeesiat, rektaalset verejooksu, hemorraagilist kõhulahtisust, melaena ja maohaavandi verejooksu
11 Kaasa arvatud erüteem, eksfoliatiivne lööve, kuumalööve, lööve, erüteemiline lööve, follikulaarne lööve, generaliseerunud lööve, makulaarne lööve, makulopapulaarne lööve, morbilliformne lööve, papulaarne lööve, sügelev lööve, vesikulaarne lööve, erütematoosne lööve
12 Kaasa arvatud pollakiuria
13 Hõlmab emakakaela verejooksu, emaka düsfunktsiooni, emaka verejooksu, suguelundite verejooksu, menometrorraagiat, menorraagiat, metrorraagiat, polümenorröad, menopausijärgset verejooksu, emaka verejooksu, tupeverejooksu
14 Hõlmab ejakulatsiooni ebaõnnestumist, ejakulatsiooni düsfunktsiooni, enneaegset seemnepurset, hilinenud ejakulatsiooni, retrograadset ejakulatsiooni
15 Kaasa arvatud asteenia.
Samuti on teatatud maitsehäiretest, pearinglusest, eufooriast, anorgasmiast ja hüponatreemiast.
c) Valitud kõrvaltoimete kirjeldus
Enesetapp / enesetapumõtted või kliiniline halvenemine: Fluoksetiinravi ajal või varsti pärast ravi lõpetamist on teatatud enesetapumõtete ja suitsidaalse käitumise juhtudest (vt lõik 4.4).
Luumurrud: Epidemioloogilised uuringud, mis viidi läbi peamiselt 50 -aastastel ja vanematel patsientidel, näitavad SSRI -de ja TCA -dega patsientidel suurenenud luumurdude riski
Selle suurenenud riski taga olev mehhanism on teadmata.
Pärast ravi lõpetamist fluoksetiiniga täheldati võõrutusnähte: Fluoksetiinravi katkestamine põhjustab tavaliselt võõrutusnähte. Kõige sagedamini on teatatud pearinglusest, sensoorsetest häiretest (sh paresteesiast), unehäiretest (sh unetus ja intensiivsed unenäod), asteeniast, erutusest või ärevusest, iiveldusest ja / või oksendamisest, värisemisest ja peavalust. .
Üldiselt on need sündmused kerged / mõõdukad ja iseenesest mööduvad, kuid mõnedel patsientidel võivad need olla rasked ja / või pikaajalised (vt lõik 4.4). Seetõttu on soovitatav ravi katkestada, vähendades annust järk -järgult, kui ravi Fluoxeren’iga ei ole enam vajalik (vt lõigud 4.2 ja 4.4).
d) Lapsed (vt lõigud 4.4 ja 5.1)
Allpool on kirjeldatud kõrvaltoimeid, mida selles populatsioonis on täheldatud spetsiifiliselt või erineva sagedusega. Nende sündmuste esinemissagedus põhineb kokkupuutel laste kliinilistes uuringutes (n = 610).
Laste kliinilistes uuringutes olid enesetapuga seotud käitumised (enesetapukatse ja enesetapumõtted), vaenulikkus (teatatud sündmused olid: viha, ärrituvus, agressiivsus, erutus, hüperaktiivsuse sündroom), maniakaalsed reaktsioonid, sealhulgas maania ja hüpomaania (ilma nendel patsientidel varem teatatud episoodidena) ) ja ninaverejooksu tekkisid sageli ja neid täheldati sagedamini antidepressantidega ravitud laste ja noorukite seas kui platseebot saanud patsientidel.
Fluoksetiini ohutust ei ole süstemaatiliselt hinnatud kroonilise ravi korral, mis kestab kauem kui 19 nädalat.
Kliinilistes uuringutes lastel on teatatud maniakaalsetest reaktsioonidest, sealhulgas maaniast ja hüpomaaniast (2,6% fluoksetiiniga ravitud patsientidest vs 0% platseebokontrolliga patsientidest), mis on enamasti põhjustanud ravi katkestamise. Nendel patsientidel ei olnud varem hüpomaania / maania episoodid.
Pärast 19 -nädalast ravi teatasid kliinilises uuringus fluoksetiiniga ravitud lastel keskmiselt 1,1 cm väiksemad kasvud (p = 0,004) ja 1,1 kg vähem (p = 0,008) võrreldes platseeboga ravitud isikutega.
Kliinilise kasutamise ajal on teatatud ka üksikutest kasvupeetuse juhtudest (vt ka lõik 5.1).
Laste populatsioonis läbi viidud kliinilistes uuringutes seostati fluoksetiinravi leeliselise fosfataasi taseme langusega.
Laste kliinilisel kasutamisel on teatatud üksikutest kõrvaltoimete juhtudest, mis võivad viidata seksuaalse küpsemise hilinemisele või seksuaalsele düsfunktsioonile (vt ka lõik 5.3).
Arvatavatest kõrvaltoimetest teatamine
Pärast ravimi müügiloa väljastamist tekkinud arvatavatest kõrvaltoimetest teatamine on oluline, kuna see võimaldab pidevalt jälgida ravimi kasu ja riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest riikliku teavitussüsteemi kaudu. "Aadress www. agenziafarmaco.gov.it/it/responsabili.
04.9 Üleannustamine -
Sümptomid
Ainuüksi fluoksetiini põhjustatud üleannustamise juhtumid on tavaliselt kerged. Üleannustamise sümptomiteks on iiveldus, oksendamine, krambid, kardiovaskulaarne düsfunktsioon, alates asümptomaatilistest arütmiatest (sh sõlme rütmi rütmihäired ja ventrikulaarsed arütmiad) või EKG muutustest, mis viitavad QT -intervalli pikenemisele kuni südame seiskumiseni (sealhulgas väga harvad torsade de pointes juhtumid), kopsufunktsiooni häired ja muutunud kesknärvisüsteemi seisundi tunnused, alates erutusest kuni koomani. Fluoksetiini üledoosist tingitud surmaga lõppenud tulemus on olnud äärmiselt haruldane.
Ravi
Soovitatav on südamefunktsiooni ja eluliste näitajate jälgimine ning üldised sümptomaatilised ja toetavad meetmed. Spetsiifilisi antidoote pole teada.
Sunnitud diurees, dialüüs, hemoperfusioon ja asendusülekanne tõenäoliselt kasu ei too. Aktiivsüsi, mida saab kasutada koos sorbitooliga, võib olla isegi tõhusam ravi kui oksendamine või maoloputus. Üleannustamise ravimisel kaaluge mitmete ravimite kaasamise võimalust. Patsiendid, kes on võtnud liiga palju tritsüklilist antidepressanti, võivad vajada pikemat aega hoolikaks arstlikuks jälgimiseks, kui nad võtavad või on hiljuti kasutanud fluoksetiini.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 "Farmakodünaamilised omadused -
Farmakoterapeutiline rühm: antidepressandid; selektiivsed serotoniini tagasihaarde inhibiitorid.
ATC -kood: N06AB03.
Fluoksetiin on selektiivne serotoniini tagasihaarde inhibiitor ja ilmselt ka selle toimemehhanism. Fluoksetiinil puudub praktiliselt igasugune afiinsus teiste retseptorite suhtes, nagu alfa1-, alfa2- ja beeta-adrenergilised ained, serotonergilised ained, dopamiinergilised I tüüpi histamiini retseptorid; muskariinid ja GABA retseptorid.
Peamised depressiooni episoodid: Kliinilised uuringud, milles võrreldi platseebot ja toimeaineid, viidi läbi depressiooni episoodidega patsientidel. Fluoksetiin on osutunud oluliselt efektiivsemaks kui platseebo, nagu näitab Hamiltoni depressiooni hindamisskaala (HAM-D). Võrreldes platseeboga põhjustas fluoksetiin nendes uuringutes oluliselt kõrgema ravivastuse (määratletud HAM-D skoori 50% vähenemisega) ja remissiooni.
Obsessiiv-kompulsiivne häire: Lühiajalistes kliinilistes uuringutes (kestusega alla 24 nädala) on fluoksetiin osutunud oluliselt efektiivsemaks kui platseebo. Terapeutilist toimet täheldati annuses 20 mg / päevas, kuid suuremad annused (40 või 60 mg / päevas) näitasid suuremat ravivastust. Pikaajalistes kliinilistes uuringutes (3 lühiajalist kliinilist uuringut, mille pikendusfaas oli retsidiivide ennetamise uuring) efektiivsust ei ole tõestatud.
Buliimia: Lühiajalistes kliinilistes uuringutes (kestus alla 16 nädala) näidati ambulatoorsetel patsientidel, kes täitsid täielikult bulimia nervosa DSM-III-R kriteeriume, fluoksetiin 60 mg ööpäevas söömishäirete vähendamisel ja platseebost oluliselt tõhusamalt. puhastamine. Pikaajalise tõhususe osas ei ole aga võimalik järeldust teha.
Kaks platseebokontrollitud kliinilist uuringut viidi läbi patsientidega, kes vastasid menstruatsioonieelse düsfoorilise häire diagnostilistele kriteeriumidele, nagu on kirjeldatud DSM-IV kohta. Patsiendid kaasati, kui nende sümptomid olid piisavalt tõsised, et häirida nende tööalast ja sotsiaalset funktsiooni ning suhteid teistega. Suukaudseid rasestumisvastaseid vahendeid kasutavad patsiendid jäeti välja. Esimeses uuringus, kus pidev annus oli 20 mg päevas 6 menstruaaltsükli jooksul, täheldati efektiivsuse esmase parameetri (ärrituvus, ärevus, düsfooria) paranemist. Teises uuringus, kus luteaalfaasis (20 mg päevas 14 päeva jooksul) manustati vahelduvaid annuseid 3 menstruaaltsükli jooksul, täheldati efektiivsuse esmase parameetri (skoor, mis põhineb häirete raskusastme igapäevasel registreerimisskaalal) paranemist. Probleemiskoori tõsiduse rekord). Siiski ei saa nendest uuringutest teha lõplikke järeldusi ravi efektiivsuse ja kestuse kohta.
05.2 "Farmakokineetilised omadused -
Imendumine
Pärast suukaudset manustamist imendub fluoksetiin seedetraktist hästi. Toidu tarbimine ei mõjuta biosaadavust.
Levitamine
Fluoksetiin seondub ulatuslikult plasmavalkudega (ligikaudu 95%) ja jaotub organismis hajusalt (jaotusruumala: 20 ... 40 l / kg). Tasakaalukontsentratsioon plasmas saavutatakse alles pärast mitmenädalast ravi. Tasakaalukontsentratsioonid pärast pikaajalist manustamist on sarnased 4-5 nädala pärast täheldatuga.
Ainevahetus
Fluoksetiinil on mittelineaarne farmakokineetiline profiil, millel on maksa esmakordne toime. Maksimaalne plasmakontsentratsioon saavutatakse tavaliselt 6 ... 8 tundi pärast manustamist. Fluoksetiini metaboliseerib ulatuslikult polümorfne ensüüm CYP2D6. Fluoksetiin metaboliseerub peamiselt maksas demetüleerimise teel aktiivseks metaboliidiks norfluoksetiiniks (demetüülfluoksetiin).
Elimineerimine
Fluoksetiini eliminatsiooni poolväärtusaeg on 4-6 päeva, norfluoksetiinil 4-16 päeva. Need pikad poolväärtusajad põhjustavad ravimi püsimist 5-6 nädala jooksul pärast selle katkestamist. Eliminatsioon toimub peamiselt neerude kaudu ( umbes 60%). Fluoksetiin eritub rinnapiima.
Riskirühmad
• Eakad: tervetel eakatel kineetilised parameetrid võrreldes noorematega ei muutu.
• Maksapuudulikkus: maksapuudulikkuse (alkohoolne tsirroos) korral pikeneb fluoksetiini ja norfluoksetiini poolväärtusaeg vastavalt 7 ja 12 päevani. Kaaluda tuleks väiksemat või harvemat annust.
• Neerupuudulikkus: pärast fluoksetiini ühekordse annuse manustamist kerge, mõõduka või täieliku (anuuria) neerupuudulikkusega patsientidele ei muutunud kineetilised parameetrid võrreldes tervete vabatahtlikega. Siiski võib pärast korduvat manustamist täheldada plasmakontsentratsiooni tasakaaluplatoo tõusu.
05.3 Prekliinilised ohutusandmed -
In vitro või loomadega läbi viidud uuringud ei näidanud kantserogeenset, mutageenset toimet ega viljakust.
06.0 FARMATSEUTILINE TEAVE -
06.1 Abiained -
FLUOXEREN 20 mg kõvakapslid: iga kõvakapsel sisaldab: maisitärklist, dimetikooni, lakitud sinist V E-131, kollast raudoksiidi E-172, titaandioksiidi E-171, želatiini
FLUOXEREN 20 mg / 5 ml suukaudne lahus: 5 ml suukaudset lahust sisaldab: bensoehapet, sahharoosi, glütseriini, piparmündimaitset, puhastatud vett
FLUOXEREN 20 mg dispergeeruvad tabletid: iga dispergeeruv tablett sisaldab: mikrokristalset tselluloosi, naatriumsahhariini, mannitooli, sorbitooli, aniisi lõhna- ja maitseainet, piparmündimaitset, kolloidset veevaba ränidioksiidi, eelželatineeritud tärklist, naatriumstearüülfumaraati, krospovidooni.
06.2 Sobimatus "-
Ei ole asjakohane.
06.3 Kehtivusaeg "-
FLUOXEREN 20 mg kõvakapslid: 3 aastat.
FLUOXEREN 20 mg dispergeeruvad tabletid: 2 aastat.
FLUOXEREN 20 mg / 5 ml suukaudne lahus: 2 aastat.
06.4 Säilitamise eritingimused -
FLUOXEREN 20 mg kõvakapslid ja FLUOXEREN 20 mg / 5 ml suukaudne lahus
Hoida temperatuuril kuni 25 ° C.
FLUOXEREN 20 mg dispergeeruvad tabletid
Hoida temperatuuril kuni 30 ° C.
06.5 Vahetu pakendi iseloom ja pakendi sisu -
FLUOXEREN 20 mg kõvakapslid
Toode on pakendatud blisterpakenditesse, mis koosnevad PVC (läbipaistmatu) ja alumiiniumist.
Blisterpakendis 12 kõvakapslit
Blister 28 kõvakapsliga.
FLUOXEREN 20 mg dispergeeruvad tabletid
Toode on pakendatud blisterpakenditesse, mis koosnevad ACLARist ja alumiiniumist.
Blisterpakendis 12 dispergeeruvat tabletti
Blister sisaldab 28 dispergeeruvat tabletti.
FLUOXEREN 20 mg / 5 ml suukaudne lahus
Toode on pakendatud 60 ml merevaigukollastesse klaaspudelitesse ja suletud plastkorgiga.
Kõik pakendi suurused ei pruugi olla müügil.
06.6 Kasutamis- ja käsitsemisjuhised -
FLUOXEREN 20 mg kõvakapslid:
Neelata alla närimata.
FLUOXEREN 20 mg / 5 ml suukaudne lahus:
Fluoxereni suukaudse lahuse täpse soovitatava annuse saab kergesti järgida, järgides alltoodud juhiseid:
- Sisestage doseerimispipett pudelisse, veendudes, et kolb on lõpuni sisestatud.
- Tõmmake kolbi ülespoole, kuni saavutatakse arsti soovitatud annus.
- Valage sisu klaasi ja lahjendage veega maitse järgi.
FLUOXEREN 20 mg dispergeeruvad tabletid:
Neelake alla närimata või lahustage tablett vees, maitse järgi lahjendades.
07.0 MÜÜGILOA HOIDJA -
A. Menarini Industrie Farmaceutiche Riunite s.r.l. - Via Sette Santi, 3 - Firenze
Edasimüüja: Istituto Luso Farmaco d "Italia S.p.A. - Milanofiori - Tee 6 - Hoone L - Rozzano (MI)
08.0 MÜÜGILOA NUMBER -
FLUOXEREN 20 mg kõvakapslid (12 kapslit): AIC n. 025959014
FLUOXEREN 20 mg kõvakapslid (28 kapslit): AIC n. 025959040
FLUOXEREN 20 mg / 5 ml suukaudne lahus: AIC n. 025959026
FLUOXEREN 20 mg dispergeeruvad tabletid (12 tabletti): AIC n. 025959038
FLUOXEREN 20 mg dispergeeruvad tabletid (28 tabletti): AIC n. 025959053
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV -
MÜÜGILOA UUENDAMINE
Mai 2010
ESIMENE MÜÜGILOA
FLUOXEREN 20 mg kõvakapslid (12 kapslit): oktoober 1988
FLUOXEREN 20 mg kõvakapslid (28 kapslit): veebruar 2000
FLUOXEREN 20 mg dispergeeruvad tabletid (12 tabletti): august 1999
FLUOXEREN 20 mg dispergeeruvad tabletid (28 tabletti): veebruar 2000
FLUOXEREN 20 mg / 5 ml suukaudne lahus: november 1994
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV -
Septembril 2015