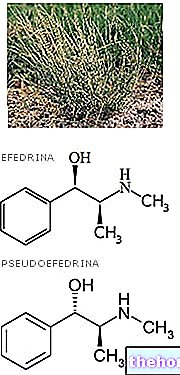
Toimeained: dipüridamool, atsetüülsalitsüülhape
AGGRENOX 200 mg + 25 mg toimeainet modifitseeritult vabastavad kõvakapslid
Näidustused Miks Aggrenoxi kasutatakse? Milleks see mõeldud on?
FARMAKOTERAPEUTILINE KATEGOORIA
Tromboosivastased ained, trombotsüütide vastased ained - dipüridamooli / atsetüülsalitsüülhappe kombinatsioon.
RAVI NÄIDUSTUSED
Insuldi ennetamine patsientidel, kellel on varasemad mööduvad isheemilised atakid või tromboosist tingitud täielik isheemiline insult (sekundaarne ennetus).
Vastunäidustused Aggrenoxi ei tohi kasutada
- Ülitundlikkus toimeainete (dipüridamool ja atsetüülsalitsüülhape), salitsülaatide või ravimi ükskõik millise abiaine suhtes.
- Patsiendid, kellel on aktiivne mao- või kaksteistsõrmiksoole haavand või kellel on hüübimishäired.
- Rasedus ja imetamine: AGGRENOX on raseduse esimesel ja teisel trimestril ning imetamise ajal üldiselt vastunäidustatud; kolmandal trimestril vastunäidustatud (vt ka "Erihoiatused").
- Selle ravimi kasutamine on vastunäidustatud alla 16 -aastastel lastel ja noortel.
- Atsetüülsalitsüülhappe sisalduse tõttu tuleb AGGRENOXi manustamist raske neerupuudulikkusega (glomerulaarfiltratsiooni kiirus alla 10 ml / min) või maksaga patsientidel vältida.
Harvaesinevate pärilike seisundite korral, mis võivad olla ravimi abiainega kokkusobimatud, on see vastunäidustatud.
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Aggrenoxi võtmist
Hoiatused atsetüülsalitsüülhappe kohta
Atsetüülsalitsüülhappe olemasolu tõttu tuleb AGGRENOX'i kasutada ettevaatusega astma, allergilise riniidi, ninapolüüpide, kroonilise või korduva mao- või kaksteistsõrmiksoole valu, neeru- või maksapuudulikkuse või glükoos-6-fosfaatdehüdrogenaasi puudulikkusega patsientidel. Enne AGGRENOX-ravi alustamist tuleb veenduda, et patsiendil ei ole varem olnud ülitundlikkusreaktsioone atsetüülsalitsüülhappe või teiste mittesteroidsete põletikuvastaste ravimite suhtes.
Kardiovaskulaarsed patoloogiad
Muude omaduste hulgas on dipüridamoolil veresooni laiendav toime. Dipüridamooli tuleb kasutada ettevaatusega patsientidel, kellel on raske koronaararteri haigus, sealhulgas ebastabiilne stenokardia või hiljutine müokardiinfarkt, ventrikulaarne väljavoolu takistus või hemodünaamiline ebastabiilsus (nt kongestiivne südamepuudulikkus).
Myasthenia gravis
Myasthenia gravis'ega patsientidel võib dipüridamooli annuse muutmisel olla vajalik raviskeemi muutmine (vt "Koostoimed").
AGGRENOXis sisalduva atsetüülsalitsüülhappe annust ei ole uuritud müokardiinfarkti sekundaarse ennetamise korral.
Lapsed ja noorukid
Atsetüülsalitsüülhappe ja Reye sündroomi vahel võib olla seos, kui seda manustatakse lastele. Seetõttu ei tohi AGGRENOXi kasutada Reye sündroomi ohu tõttu palavikuga või viirusinfektsiooniga lastel ja noorukitel. Reye sündroom on väga haruldane haigus, mis mõjutab aju ja maksa ning võib lõppeda surmaga.
Eakad kodanikud
Üle 70 -aastased inimesed, eriti samaaegse ravi korral, peaksid seda ravimit kasutama alles pärast arstiga konsulteerimist.
Koostoimed Millised ravimid või toidud võivad muuta Aggrenoxi toimet
Rääkige oma arstile või apteekrile, kui olete hiljuti kasutanud mingeid muid ravimeid, isegi ilma retseptita.
Mittesteroidsed põletikuvastased ravimid (NSAID) / Kortikosteroidid / Alkohol
Seedetrakti kõrvaltoimed suurenevad, kui atsetüülsalitsüülhapet manustatakse koos MSPVA -de, kortikosteroidide või kroonilise alkoholitarbimisega.
Dipüridamooli seostamine atsetüülsalitsüülhappega ei suurenda verejooksude esinemissagedust.
Ibuprofeeni, kuid kindlasti mitte teiste MSPVA -de või paratsetamooli samaaegne manustamine võib vähendada kardiovaskulaarse riskiga patsientidel aspiriini kasulikke kardiovaskulaarseid toimeid.
Ained, mis mõjutavad vere hüübimist
Kui dipüridamooli kasutatakse koos mõne muu hüübimist mõjutava ainega, näiteks antikoagulantide ja trombotsüütide vastaste ravimitega, tuleb arvesse võtta nende ravimite pakendi infolehtedes kirjeldatud ettevaatusabinõusid, hoiatusi ja taluvust.
On näidatud, et atsetüülsalitsüülhape suurendab verejooksu riski, kui seda manustatakse koos antikoagulantide, trombotsüütide vastaste ravimite, selektiivsete serotoniini tagasihaarde inhibiitorite (SSRI) või anagreliidiga.
Kui dipüridamooli manustatakse koos varfariiniga, ei ole verejooks sagedasem ega intensiivsem kui ainult varfariini kasutamisel.
Antikonvulsandid
On näidatud, et atsetüülsalitsüülhape suurendab valproehappe ja fenütoiini toimet, suurendades kõrvaltoimete riski.
Adenosiin
Dipüridamool suurendab adenosiini taset veres ja kardiovaskulaarset toimet, mistõttu tuleb kaaluda adenosiini annuse muutmise otstarbekust.
Antihüpertensiivsed ravimid
Dipüridamool võib suurendada antihüpertensiivsete ravimite hüpotensiivset toimet.
Koliinesteraasi inhibiitorid
Dipüridamool võib neutraliseerida koliinesteraasi inhibiitorravimite antikolinesteraasi toimet ja halvendada müasteenia juhtumeid.
Hüpoglükeemilised ravimid / metotreksaat
Atsetüülsalitsüülhappe samaaegne manustamine võib suurendada hüpoglükeemiliste ravimite toimet ja metotreksaadi toksilisust.
Spironolaktoon / Uricosuric ained
Atsetüülsalitsüülhape võib vähendada spironolaktooni natriureetilist toimet ja pärssida urikosuuriliste ravimite (nt probenetsiid, sulfiinpürasoon) toimet.
Ravi mõju võib muutuda, kui atsetüülsalitsüülhapet võetakse koos teiste ravimitega, näiteks:
- antikoagulandid (nt varfariin);
- äratõukereaktsiooni vastased ravimid (nt tsüklosporiin, takroliimus);
- antihüpertensiivsed ravimid (nt diureetikumid ja AKE inhibiitorid);
- valuvaigistid ja põletikuvastased ravimid (nt steroidid, mittesteroidsed põletikuvastased ravimid);
- podagra ravimid (probenetsiid);
- vähivastased ja reumatoidartriidi ravimid (metotreksaat).
Enne atsetüülsalitsüülhappe kasutamist rääkige oma arstile, kui te võtate mingeid muid ravimeid (kaasa arvatud eneseravimid).
Hoiatused Oluline on teada, et:
Verejooks
Verejooksu ohu tõttu, nagu ka teiste trombotsüütide vastaste ainete puhul, tuleb AGGRENOXi kasutada ettevaatusega suurenenud verejooksuohuga patsientidel, neid tuleb hoolikalt jälgida verejooksu nähtude, sealhulgas varjatud verejooksu suhtes (vt „Koostoimed“).
Patsiente, kes võtavad samaaegselt ravimeid, mis võivad suurendada verejooksu riski, nagu antikoagulandid, trombotsüütide vastased ained, selektiivsed serotoniini tagasihaarde inhibiitorid (SSRI -d), anagreliidi, tuleb ravida ettevaatusega (vt „Koostoimed“).
Sapiteede häired
On teatatud vähesest juhtumist, kus konjugeerimata dipüridamooli on sapikividesse lisatud erinevas koguses (kuni 70% kivi kuivmassist). Need patsiendid olid kõik eakad, neil oli esinenud tõusvat kolangiiti ja neid oli mitu aastat ravitud suukaudse dipüridamooliga. Nendel patsientidel ei ole näidatud, et dipüridamool vallandab sapikivid. Võimalik, et konjugeeritud dipüridamooli bakteriaalne deglükuronidatsioon sapis võib olla mehhanism, mis vastutab dipüridamooli esinemise eest sapikivides.
Peavalu või migreen
Peavalu või migreeni, mis võivad tekkida eriti AGGRENOX -ravi alguses, ei tohi ravida atsetüülsalitsüülhappe valuvaigistavate annustega.
Stressitest intravenoosse dipüridamooliga
Kliiniline kogemus näitab, et suukaudse dipüridamooliga ravitavad patsiendid, kellele tuleb teha ka intravenoosse dipüridamooliga ravimite stressitest, peaksid lõpetama suukaudse ravi dipüridamooli sisaldavate ravimitega 24 tundi enne intravenoosse dipüridamoolravi alustamist. intravenoosne dipüridamool võib kahjustada testi tundlikkust.
Kasutage raseduse või rinnaga toitmise ajal
Enne mis tahes ravimi kasutamist pidage nõu oma arsti või apteekriga.
Rasedus
Dipüridamooli ja atsetüülsalitsüülhappe väikeste annuste ohutuse kohta raseduse ajal ei ole piisavalt tõendeid. Seetõttu tohib AGGRENOXi raseduse esimesel ja teisel trimestril manustada ainult juhul, kui arst peab seda oodatava kasu ja võimalike riskide seisukohast oluliseks. Lisaks ei tohi AGGRENOXi raseduse kolmandal trimestril manustada (vt "Vastunäidustused").
Toitmisaeg
Dipüridamool ja salitsülaadid erituvad rinnapiima. Seetõttu tohib AGGRENOXi imetavatele naistele manustada ainult äärmise vajaduse korral.
Viljakus
Uuringuid ravimi mõju kohta inimese fertiilsusele ei ole läbi viidud.
Toime autojuhtimise ja masinate käsitsemise võimele
Uuringuid ravimi toime kohta autojuhtimisele ja masinate käsitsemise võimele ei ole läbi viidud.
Siiski on kliinilistes uuringutes täheldatud selliseid sümptomeid nagu pearinglus ja segasus (vt „Kõrvaltoimed“). Seetõttu soovitatakse patsientidel autojuhtimisel ja masinate käsitsemisel olla ettevaatlik.
Kui patsientidel tekivad sellised sümptomid, peaksid nad vältima potentsiaalselt ohtlikke tegevusi, nagu autojuhtimine või masinatega töötamine.
Oluline teave mõningate AGGRENOXi koostisainete kohta
AGGRENOX sisaldab laktoosi ja sahharoosi. Kui arst on teile öelnud, et te ei talu teatud suhkruid, võtke enne selle ravimi kasutamist ühendust oma arstiga.
Annustamine ja kasutusviis Kuidas Aggrenoxi kasutada: Annustamine
Suukaudseks manustamiseks. Soovitatav annus on 1 kapsel kaks korda päevas, tavaliselt 1 hommikul ja 1 õhtul, eelistatavalt söögi ajal.
Kapslid tuleb tervelt alla neelata ilma närimata.
Kui teil on lisaküsimusi AGGRENOXi kasutamise kohta, pidage nõu oma arsti või apteekriga.
Üleannustamine Mida teha, kui olete võtnud liiga palju Aggrenoxi
AGGRENOXi liigse annuse juhusliku allaneelamise / võtmise korral teavitage sellest kohe oma arsti või minge lähimasse haiglasse.
Sümptomid
Arvestades dipüridamooli ja atsetüülsalitsüülhappe annuste suhet, domineerivad üleannustamise korral dipüridamooli nähud ja sümptomid.
Kuna teatatud juhtumeid on vähe, on dipüridamooli üleannustamise kogemus piiratud. Oodata on selliseid sümptomeid nagu kuumad aistingud, õhetus, higistamine, rahutus, nõrkustunne, pearinglus ja stenokardiavalud. Võib täheldada vererõhu langust ja tahhükardiat.
Atsetüülsalitsüülhappe tagasihoidliku ägeda üleannustamise tunnused ja sümptomid on hüperventilatsioon, sumin, iiveldus, oksendamine, nägemis- ja kuulmishäired, pearinglus ja segasus. Raske mürgistuse korral võib täheldada deliiriumi, värisemist, hingeldust, higistamist. Verejooks, dehüdratsioon, häired happe-aluse tasakaalus ja vere elektrolüütide koostises, hüpotermia ja kooma. Pearinglus ja helin kõrvus võib olla üleannustamise sümptom, eriti eakatel patsientidel.
Teraapia
Soovitatav on sümptomaatiline ravi. Tuleb kaaluda maoloputust. Ksantiiniderivaatide (nt aminofülliin) manustamine võib neutraliseerida dipüridamooli üleannustamise hemodünaamilisi mõjusid. Kuna dipüridamool on laialt levinud kudedes ja domineeriv maksa kaudu, ei ole selle kiirendatud eemaldamiseks peaaegu kättesaadav.
Kui teil on lisaküsimusi AGGRENOXi kasutamise kohta, pidage nõu oma arsti või apteekriga.
Kõrvaltoimed Millised on Aggrenoxi kõrvaltoimed
Nagu kõik ravimid, võib ka AGGRENOX põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki.
AGGRENOXi kõrvaltoimed, mis on loetletud süsteemse orgaanilise klassi järgi:
Vere ja lümfisüsteemi häired
Trombotsütopeenia (trombotsüütide arvu vähenemine), aneemia, varjatud seedetrakti verejooksust tingitud rauapuuduse aneemia.
Immuunsüsteemi häired
Ülitundlikkusreaktsioonid, sealhulgas lööve, urtikaaria, raske bronhospasm ja angioödeem.
Närvisüsteemi häired
Intrakraniaalne verejooks, pearinglus, peavalu, isegi migreen (eriti ravi alguses).
Silma häired
Silma hemorraagia.
Südame patoloogiad
Tahhükardia, südame isheemiatõve sümptomite halvenemine, minestus.
Vaskulaarsed patoloogiad
Hüpotensioon, kuumahood.
Hingamisteede, rindkere ja mediastiinumi häired
Ninaverejooks.
Seedetrakti häired
Oksendamine, iiveldus, kõhulahtisus, düspepsia, maohaavand, kaksteistsõrmiksoole haavand, erosiooniga gastriit, seedetrakti verejooks, kõhuvalu.
Naha ja nahaaluskoe kahjustused
Naha verejooks, sealhulgas verevalumid, verevalumid ja hematoom.
Lihas -skeleti süsteemi, sidekoe häired
Müalgia.
Diagnostilised testid
Pikaajaline veritsusaeg.
Vigastus, mürgistus ja protseduurilised komplikatsioonid
Menetlusjärgne hemorraagia, protseduuriline verejooks.
Üksikute toimeainete teadaolevad kõrvaltoimed on järgmised, samuti loetakse need AGGRENOXi jaoks ette nähtud.
Dipüridamool:
Täiendavad kõrvaltoimed, mida on teatatud ainult dipüridamooli kasutamisel, on järgmised:
Dipüridamooli on teatatud sapikividest.
Atsetüülsalitsüülhape:
Täiendavad kõrvaltoimed, mida on teatatud ainult atsetüülsalitsüülhappe kasutamisel, on järgmised:
Vere ja lümfisüsteemi häired
Hajutatud intravaskulaarne hüübimine, koagulopaatia.
Immuunsüsteemi häired
Anafülaktilised reaktsioonid (eriti astmahaigetel).
Ainevahetus- ja toitumishäired
Hüpoglükeemia (lapsed), hüperglükeemia, janu, dehüdratsioon, hüperkaleemia, metaboolne atsidoos, hingamisteede alkaloos.
Psühhiaatrilised häired
Segadusseisund.
Närvisüsteemi häired
Erutus, ajuturse, letargia, krambid. Kõrva ja labürindi kahjustused Tinnitus, kurtus.
Südame patoloogiad
Arütmia.
Hingamisteede, rindkere ja mediastiinumi häired
Hingeldus, igemete verejooks, kõriturse, hüperventilatsioon, kopsuturse, tahhüpnoe.
Seedetrakti häired
Perforeeritud maohaavand, perforeeritud kaksteistsõrmiksoole haavand, melaena, hematemees, pankreatiit.
Maksa ja sapiteede häired
Hepatiit, Reye sündroom.
Naha ja nahaaluskoe kahjustused
Polümorfne erüteem.
Lihas -skeleti süsteemi, sidekoe häired
Rabdomüolüüs.
Neerude ja kuseteede häired
Neerupuudulikkus, interstitsiaalne nefriit, neerude papillaarne nekroos, proteinuuria.
Rasedus, sünnitusjärgne periood ja perinataalsed seisundid
Pikaajaline rasedus, pikaajaline sünnitus, väikelapsed, surnultsünd, verejooks raseduse ajal, sünnitusjärgne verejooks.
Üldised häired ja manustamiskoha reaktsioonid
Palavik, hüpotermia.
Diagnostilised testid
Ebanormaalsed maksafunktsiooni testid, suurenenud kusihappe sisaldus veres (võib põhjustada podagrahooge), pikenenud protrombiiniaeg.
Pakendi infolehel olevate juhiste järgimine vähendab kõrvaltoimete riski.
Kõrvaltoimetest teatamine
Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti või apteekriga, sealhulgas selles infolehes loetlemata. Kõrvaltoimetest võib ka ise teavitada riikliku teavitussüsteemi kaudu aadressil www.agenziafarmaco.it/it/responsabili. Kõrvaltoimetest teatades saate aidata saada rohkem teavet selle ravimi ohutuse kohta.
Aegumine ja säilitamine
Hoiatus: ärge kasutage ravimit pärast kõlblikkusaega, mis on märgitud pakendil.
Kõlblikkusaeg viitab puutumatus pakendis olevale tootele, mis on õigesti hoitud.
Hoida temperatuuril kuni 30 ° C, hoida pudel niiskuse eest kaitstult suletuna.
HOIDKE AGGRENOX LASTE EEST KÄTTESAAMATUS KOHAS.
Ravimeid ei tohi ära visata kanalisatsiooni kaudu ega koos majapidamisprügiga. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
Muu info
KOOSTIS
Üks kapsel sisaldab: Toimeained: dipüridamool 200 mg; atsetüülsalitsüülhape 25 mg.
Abiained: viinhape, povidoon, metakrüülhappe-metüülmetakrülaadi kopolümeer (1: 2), talk, araabikummi, hüpromelloosftalaat, hüpromelloos, triatsetiin, dimetikoon 350, steariin / palmitiinhape, laktoosmonohüdraat, alumiiniumstearaat, kolloidne ränidioksiid, , mikrokristalne tselluloos, sahharoos, E 171; kapsel (kõva): želatiin, E 171, E 172, puhastatud vesi.
RAVIMVORM JA SISU
Modifitseeritud vabanemisega kõvad kapslid. Pakendis: 50, 60 kapslit.
Kõik pakendi suurused ei pruugi olla müügil.
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS
AGGRENOX 200 MG + 25 MG KÕVALT MUUDETUD VABASTAMISKAPSLID
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Üks kapsel sisaldab:
dipüridamool 200 mg
atsetüülsalitsüülhape 25 mg
Teadaolevat toimet omavad abiained: üks kapsel sisaldab 53 mg laktoosi ja 11,3 mg sahharoosi
Abiainete täielik loetelu vt lõik 6.1
03.0 RAVIMVORM
Modifitseeritud vabanemisega kõvad kapslid.
04.0 KLIINILINE TEAVE
04.1 Näidustused
AGGRENOX on näidustatud insuldi profülaktikaks patsientidel, kellel on varasemad mööduvad isheemilised atakid või tromboosist tingitud täielik isheemiline insult (sekundaarne ennetus).
04.2 Annustamine ja manustamisviis
Soovitatav annus on üks kapsel kaks korda päevas, tavaliselt üks kord hommikul ja üks kord õhtul, eelistatavalt söögi ajal.
Kapslid tuleb tervelt alla neelata ilma närimata.
04.3 Vastunäidustused
• Ülitundlikkus toimeainete, salitsülaatide või ravimi ükskõik millise abiaine suhtes.
• aktiivse mao- või kaksteistsõrmiksoole haavandiga või hüübimishäiretega patsiendid.
• Rasedus ja imetamine: AGGRENOX on raseduse esimesel ja teisel trimestril ning imetamise ajal üldiselt vastunäidustatud, kolmandal trimestril vastunäidustatud (vt lõik 4.6).
• Selle ravimi kasutamine on vastunäidustatud alla 16 -aastastel lastel ja noortel.
• Atsetüülsalitsüülhappe sisalduse tõttu tuleb AGGRENOXi manustamist raske neerupuudulikkusega (glomerulaarfiltratsiooni kiirus alla 10 ml / min) või maksaga patsientidel vältida (vt ka lõik 5.2).
Harvaesinevate pärilike seisundite korral, mis võivad olla ravimi abiainega kokkusobimatud, on see vastunäidustatud.
04.4 Erihoiatused ja asjakohased ettevaatusabinõud kasutamisel
Verejooks
Verejooksu ohu tõttu, nagu ka teiste trombotsüütide vastaste ainete puhul, tuleb AGGRENOXi kasutada ettevaatusega patsientidel, kellel on suurenenud verejooksu oht, neid tuleb hoolikalt jälgida veritsusnähtude, sealhulgas varjatud verejooksu suhtes (vt lõik 4.5).
Patsiente, kes võtavad samaaegselt ravimeid, mis võivad suurendada verejooksu riski, nagu antikoagulandid, trombotsüütide vastased ained, selektiivsed serotoniini tagasihaarde inhibiitorid (SSRI -d) või anagreliid, tuleb ravida ettevaatusega (vt lõik 4.5).
Kardiovaskulaarsed patoloogiad
Muude omaduste hulgas on dipüridamoolil veresooni laiendav toime. Dipüridamooli tuleb kasutada ettevaatusega patsientidel, kellel on raske koronaararteri haigus, sealhulgas ebastabiilne stenokardia või hiljutine müokardiinfarkt, ventrikulaarne väljavoolu takistus või hemodünaamiline ebastabiilsus (nt kongestiivne südamepuudulikkus).
AGGRENOXis sisalduva atsetüülsalitsüülhappe annust ei ole uuritud müokardiinfarkti sekundaarse ennetamise korral.
Myasthenia gravis
Myasthenia gravis'ega patsientidel võib dipüridamooli annuse muutmise korral osutuda vajalikuks raviskeemi muutmine (vt lõik 4.5).
Sapiteede häired
On teatatud vähesest juhtumist, kus konjugeerimata dipüridamooli on sapikividesse lisatud erinevas koguses (kuni 70% kivi kuivmassist). Need patsiendid olid kõik eakad, neil oli esinenud tõusvat kolangiiti ja neid oli mitu aastat ravitud suukaudse dipüridamooliga. Nendel patsientidel ei ole näidatud, et dipüridamool vallandab sapikivid. Võimalik, et konjugeeritud dipüridamooli bakteriaalne deglükuronidatsioon sapis võib olla mehhanism, mis vastutab dipüridamooli esinemise eest sapikivides.
Peavalu või migreen
Peavalu või migreeni, mis võivad tekkida eriti AGGRENOX -ravi alguses, ei tohi ravida atsetüülsalitsüülhappe valuvaigistavate annustega.
Ülitundlikkus
Lisaks tuleb olla ettevaatlik MSPVA -de suhtes ülitundlikel patsientidel.
Hoiatused atsetüülsalitsüülhappe kohta
Atsetüülsalitsüülhappe olemasolu tõttu tuleb AGGRENOX'i kasutada ettevaatusega astma, allergilise riniidi, ninapolüüpide, kroonilise või korduva mao- või kaksteistsõrmiksoole valu, neeru- või maksapuudulikkuse (vt lõik 5.2) või glükoos-6-fosfaadi puudulikkusega patsientidel. dehüdrogenaas.
Lapsed ja noorukid
Atsetüülsalitsüülhappe ja Reye sündroomi vahel võib olla seos, kui seda manustatakse lastele. Seetõttu ei tohi AGGRENOXi kasutada Reye sündroomi ohu tõttu palavikuga või viirusinfektsiooniga lastel ja noorukitel. Reye sündroom on väga haruldane haigus, mis mõjutab aju ja maksa ning võib lõppeda surmaga.
Eakad kodanikud
Üle 70 -aastased inimesed, eriti samaaegse ravi korral, peaksid seda ravimit kasutama alles pärast arstiga konsulteerimist.
Stressitest intravenoosse dipüridamooliga
Kliiniline kogemus näitab, et suukaudse dipüridamooliga ravitavad patsiendid, kellele tuleb teha ka intravenoosse dipüridamooliga ravimite stressitest, peaksid lõpetama suukaudse ravi dipüridamooli sisaldavate ravimitega 24 tundi enne intravenoosse dipüridamoolravi alustamist. intravenoosne dipüridamool võib kahjustada testi tundlikkust.
Hoiatused mõne AGGRENOXi koostisosa kohta
Üks kapsel sisaldab 53 mg laktoosi ja 11,3 mg sahharoosi, mis moodustab maksimaalse soovitatava ööpäevase annuse korral 106 mg laktoosi ja 22,6 mg sahharoosi: patsiendid, kellel on harvaesinev pärilik fruktoosi- ja / või galaktoositalumatus, laktaasipuudus või glükoosi- galaktoosi imendumishäire või sahharaasi isomaltaasi puudulikkus ei tohi seda ravimit võtta.
04.5 Koostoimed teiste ravimitega ja muud koostoimed
Mittesteroidsed põletikuvastased ravimid (MSPVA-d) / Kortikosteroidid / Alkohol
Seedetrakti kõrvaltoimed suurenevad, kui atsetüülsalitsüülhapet manustatakse koos MSPVA -de, kortikosteroidide või kroonilise alkoholitarbimisega.
Ibuprofeeni, kuid kindlasti mitte teiste MSPVA -de või paratsetamooli samaaegne manustamine võib vähendada kardiovaskulaarse riskiga patsientidel aspiriini kasulikke kardiovaskulaarseid toimeid.
Ained, mis mõjutavad vere hüübimist
Kui dipüridamooli kasutatakse koos mõne muu hüübimist mõjutava ainega, näiteks antikoagulantide ja trombotsüütide vastaste ravimitega, tuleb arvesse võtta nende ravimite ohutusprofiili.
On näidatud, et atsetüülsalitsüülhape suurendab verejooksu riski, kui seda manustatakse koos antikoagulantide, trombotsüütidevastaste ravimite, selektiivsete serotoniini tagasihaarde inhibiitorite (SSRI) või anagreliidiga.
Dipüridamooli seostamine atsetüülsalitsüülhappega ei suurenda verejooksude esinemissagedust.
Kui dipüridamooli manustatakse koos varfariiniga, ei ole verejooks sagedasem ega intensiivsem kui ainult varfariini kasutamisel.
Antikonvulsandid
On näidatud, et atsetüülsalitsüülhape suurendab valproehappe ja fenütoiini toimet, suurendades kõrvaltoimete riski.
Adenosiin
Dipüridamool suurendab adenosiini taset veres ja kardiovaskulaarset toimet, mistõttu tuleb kaaluda adenosiini annuse muutmise otstarbekust.
Antihüpertensiivsed ravimid
Dipüridamool võib suurendada antihüpertensiivsete ravimite hüpotensiivset toimet.
Koliinesteraasi inhibiitorid
Dipüridamool võib neutraliseerida koliinesteraasi inhibiitorite ravimite antikolinesteraasi toimet ja võib halvendada müasteenia juhtumeid (vt lõik 4.4).
Hüpoglükeemilised ravimid / metotreksaat
Atsetüülsalitsüülhappe samaaegne manustamine võib suurendada hüpoglükeemiliste ravimite toimet ja metotreksaadi toksilisust.
Spironolaktoon / Uricosuric ained
Atsetüülsalitsüülhape võib vähendada spironolaktooni natriureetilist toimet ja pärssida urikosuuriliste ravimite (nt probenetsiid, sulfiinpürasoon) toimet.
Eksperimentaalsed andmed näitavad, et ibuprofeen võib ravimite samaaegsel manustamisel pärssida atsetüülsalitsüülhappe väikeste annuste toimet trombotsüütide agregatsioonile. Siiski ei võimalda piiratud andmed ja ebakindlus nende kasutamise kohta kliinilises olukorras teha kindlaid järeldusi. ibuprofeen; tundub, et ibuprofeeni juhuslikul kasutamisel ei ole kliiniliselt olulist toimet (vt lõik 5.1).
04.6 Rasedus ja imetamine
Rasedus
Kuigi prekliinilised uuringud ei ole näidanud ohtu tervisele (vt lõik 5.3), ei ole piisavalt tõendeid dipüridamooli ja väikese annuse atsetüülsalitsüülhappe ohutuse kohta raseduse ajal. Seetõttu tohib AGGRENOXi raseduse esimesel ja teisel trimestril manustada ainult juhul, kui arst peab seda oodatava kasu ja võimalike riskide seisukohast oluliseks.
AGGRENOX on vastunäidustatud ka raseduse kolmandal trimestril.
Toitmisaeg
Dipüridamool ja salitsülaadid erituvad rinnapiima (vt lõigud 5.2 ja 5.3).
Seetõttu tohib AGGRENOXi imetavatel naistel manustada ainult äärmise vajaduse korral.
Viljakus
Uuringuid ravimi mõju kohta inimese fertiilsusele ei ole läbi viidud. Dipüridamooli või atsetüülsalitsüülhappe prekliinilistes uuringutes ei täheldatud fertiilsuse halvenemist (vt lõik 5.3).
04.7 Mõju autojuhtimise ja masinate käsitsemise võimele
Uuringuid ravimi toime kohta autojuhtimisele ja masinate käsitsemise võimele ei ole läbi viidud.
Siiski tuleb patsiente hoiatada, et kliinilistes uuringutes on teatatud sellistest sümptomitest nagu pearinglus ja segasus. Seetõttu tuleb autojuhtimisel ja masinate käsitsemisel olla ettevaatlik.
Kui patsientidel tekivad sellised sümptomid, peaksid nad vältima potentsiaalselt ohtlikke tegevusi, nagu autojuhtimine või masinatega töötamine.
04.8 Kõrvaltoimed
Ohutusprofiili kokkuvõte
AGGRENOXi ohutusprofiili määratlemiseks kasutati kahe suuremahulise uuringu (ESPS-2, PRoFESS) tulemusi, milles osales kokku 26 934 patsienti, kellest 11 831 määrati AGGRENOXi ravigruppi. Need andmed on integreeritud AGGRENOXi laialdase turustusjärgse kogemusega.
Kõige sagedamini teatatud kõrvaltoimed on peavalu, pearinglus ja seedetrakti häired, nagu düspepsia, kõhulahtisus, iiveldus ja kõhuvalu. Kõige olulisemad AGGRENOXi kasutamisega seotud tõsised kõrvaltoimed olid verejooksud.
Kõrvaltoimete tabel
AGGRENOXi kasutamise ajal ESPS-2 ja PRoFESS uuringutes ning spontaanse teatamise tulemusena teatati järgmistest kõrvaltoimetest.
1 Ainult dipüridamooli teadaolevad kõrvaltoimed
2 Atsetüülsalitsüülhappe monoteraapia teadaolevad kõrvaltoimed
Valitud kõrvaltoimete kirjeldus
Kõige olulisemad AGGRENOXi kasutamisega seotud tõsised kõrvaltoimed olid verejooksud. ESPS-2 ja PRoFESS uuringute andmeid hinnati verejooksude, sealhulgas suurte verejooksude suhtes. Verejooksud klassifitseeriti. Nagu iga verejooks, raske verejooks, intrakraniaalne verejooks ja seedetrakti verejooks:
ESPS-2 kontrollitud uuringus raviti 1650 patsienti AGGRENOXi rühmas (100%) ja 1649 patsienti platseeborühmas (100%). Keskmine ravi kestus oli 1,4 aastat. Verejooksude üldine esinemissagedus oli AGGRENOX -i rühmas 8,7% ja platseeborühmas 4,5%. Raske verejooksu esinemissagedus oli vastavalt 1,6% ja 0,4%. Intrakraniaalse verejooksu esinemissagedus oli vastavalt 0,6% ja 0,4%, seedetrakti verejooks vastavalt 4,3% ja 2,6%.
PRoFESS -uuringus raviti 10 055 patsienti AGGRENOXi rühmas (100%). Keskmine ravi kestus oli 1,9 aastat. Verejooksu üldine esinemissagedus oli 5,3%. Tõsise verejooksu esinemissagedus oli 3,3%. Intrakraniaalse verejooksu esinemissagedus oli 1,2%(sealhulgas silmasisene verejooks (0, 2%)), seedetrakti verejooks aga 1,9%.
Arvatavatest kõrvaltoimetest teatamine
Pärast ravimi müügiloa väljastamist tekkinud arvatavatest kõrvaltoimetest teatamine on oluline, kuna see võimaldab pidevalt jälgida ravimi kasu ja riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest riikliku teavitussüsteemi kaudu. "Aadress www. agenziafarmaco.gov.it/it/responsabili.
04.9 Üleannustamine
Sümptomid
Arvestades dipüridamooli ja atsetüülsalitsüülhappe annuste suhet, domineerivad üleannustamise korral dipüridamooli nähud ja sümptomid.
Kuna teatatud juhtumeid on vähe, on dipüridamooli üleannustamise kogemus piiratud. Oodata on selliseid sümptomeid nagu kuumustunne, õhetus, higistamine, rahutus, nõrkus, pearinglus ja stenokardia. Võib täheldada vererõhu langust ja tahhükardiat.
Atsetüülsalitsüülhappe tagasihoidliku ägeda üleannustamise tunnused ja sümptomid on hüperventilatsioon, sumin, iiveldus, oksendamine, nägemise ja kuulmise häired, pearinglus ja segasus.
Raske mürgistuse korral võib täheldada deliiriumi, värisemist, hingeldust, higistamist, verejooksu, dehüdratsiooni, happe-aluse tasakaalu ja vere elektrolüütide koostise häireid, hüpotermiat ja koomat.
Pearinglus ja helin kõrvus võib olla üleannustamise sümptom, eriti eakatel patsientidel.
Teraapia
Soovitatav on sümptomaatiline ravi. Tuleb kaaluda maoloputust. Ksantiini derivaatide (nt: aminofülliin) manustamine võib neutraliseerida dipüridamooli üleannustamise hemodünaamilisi mõjusid. Kuna dipüridamool on laialt levinud kudedes ja domineeriv maksa kaudu, ei ole selle kiirendatud eemaldamiseks peaaegu kättesaadav.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 Farmakodünaamilised omadused
Farmakoterapeutiline rühm: tromboosivastased ained, trombotsüütide vastased ained; ATC -kood: B01AC.
Atsetüülsalitsüülhappe / dipüridamooli kombinatsiooni tromboosivastane toime põhineb erinevatel biokeemilistel mehhanismidel.
L "atsetüülsalitsüülhape inaktiveerib pöördumatult tsüklooksügenaasi ensüümi trombotsüütides, takistades seeläbi tromboksaan A2 tootmist, mis on tugev trombotsüütide agregatsiooni ja vasokonstriktsiooni indutseerija.
The dipüridamool pärsib adenosiini omastamist erütrotsüütides, trombotsüütides ja endoteelirakkudes in vitro ja in vivo; pärssimine on maksimaalselt ligikaudu 80% ja see sõltub terapeutiliste kontsentratsioonide (0,5 ... 2 mcg / ml) annusest. Järelikult suureneb trombotsüütide A2 retseptorile mõjuv adenosiini kohalik kontsentratsioon, stimuleerides trombotsüütide adenüültsüklaasi ja suurendades seeläbi tsüklilise adenosiinmonofosfaadi (AMPc) taset trombotsüütides.
Seetõttu on trombotsüütide agregatsioon pärsitud erinevatele stiimulitele, nagu trombotsüütide aktiveeriv faktor (PAF), kollageen ja adenosiindifosfaat (ADP). Vähendatud trombotsüütide agregatsioon vähendab trombotsüütide tarbimist normaalsele tasemele. Lisaks on adenosiinil veresooni laiendav toime ja see on üks mehhanismidest, mille abil dipüridamool põhjustab veresoonte laienemist.
Insuldiga patsientidel on näidatud, et dipüridamool vähendab trombotsüütides esinevate pindmiste protrombootiliste valkude (PAR-1: trombiini retseptor) tihedust, samuti vähendab c-reaktiivse valgu (CRP) ja von Willebrandi faktori (vWF) taset.) . In vitro uuringud on näidanud, et dipüridamool pärsib selektiivselt põletikulisi tsütokiine (MCP-1 ja MMP-9), mis tulenevad trombotsüütide ja monotsüütide interaktsioonist.
Farmakodünaamika
Dipüridamool inhibeerib fosfodiesteraasi (PDE) erinevates kudedes.
Kuigi AMPc-PDE pärssimine on nõrk, pärsivad dipüridamooli terapeutilised tasemed tsüklilist guanosiinmonofosfaat-PDE-d (GMPc-PDE), suurendades seeläbi "EDRF-i (endoteelist saadud lõõgastav tegur) toodetud GMPc suurenemist", mis on identifitseeritud kui lämmastikoksiid (NO )).
Dipüridamool suurendab kudede plasminogeeni aktivaatori vabanemist mikrovaskulaarsetest endoteelirakkudest ja on näidanud, et see suurendab annusest sõltuval viisil endoteelirakkude antitrombootilisi omadusi trombi tekkimisel külgneval subendoteliaalsel maatriksil. Dipüridamool on võimas puhastusvahend oksi- ja peroksiradikaalidest.
Dipüridamool stimuleerib ka prostatsükliini biosünteesi ja vabanemist endoteeli poolt ning vähendab subendoteeli struktuuride trombogeensust, suurendades kaitsva vahendaja 13-HODE (13-hüdroksüoktadekadieenhape) kontsentratsiooni.
Kui atsetüülsalitsüülhape pärsib ainult trombotsüütide agregatsiooni, siis dipüridamool pärsib ka trombotsüütide aktivatsiooni ja adhesiooni. Seetõttu on atsetüülsalitsüülhappe ja dipüridamooli tromboosivastane toime aditiivne.
Kliinilised uuringud
AGGRENOXi uuriti 24-kuulises topeltpimedas platseebo-kontrollitud uuringus (European Stroke Prevention Study 2, ESPS2), milles 6 602 patsiendil esines kolme kuu jooksul enne registreerimist isheemiline insult või mööduv isheemiline atakk (TIA).
Patsiendid randomiseeriti ühte neljast ravigrupist: AGGRENOX (ASA / pikendatud vabanemisega dipüridamool) 25 mg / 200 mg; ainult toimeainet prolongeeritult vabastav dipüridamool (ER-DP) 200 mg; ASA 25 mg üksi või platseebo. Patsiendid said ühe kapsli kaks korda päevas (hommikul ja õhtul).
Efektiivsuse hindamine hõlmas pimeda haigestumuse ja suremuse rühma insuldi (surmaga lõppenud või mitte-surmav) ja surma (mis tahes põhjusel) analüüse. AGGRENOX ESPS-2-s vähendas insuldi riski 23,1% võrreldes ASA-ga 50 mg päevas (p = 0,006) ja vähendas insuldiriski 24,7% võrreldes dipüridamooli vabanemisega. Pikenenud 400 mg päevas (p = 0,002) ). AGGRENOX vähendas insuldi riski 37% võrreldes platseeboga (lk
ESPS-2 uuringu tulemusi toetab Euroopa / Austraalia insuldi ennetamise uuring pöörduva isheemia uuringus (ESPRIT), milles uuriti 400 mg dipüridamooli kombineeritud ravi päevas (83% patsientidest, keda raviti pikendatud dipüridamooli) ja ASA 30-325 mg päevas. Uuringusse kaasati kokku 2739 patsienti, kellel oli olnud arteriaalne isheemiline insult, 1376 ainult ASA rühmas ja 1363 ASA pluss dipüridamooli rühmas. Peamine tulemus oli surma põhjustamine kõikidest veresoonkonna põhjustest, mittefataalne insult, mittefataalne müokardiinfarkt või suure verejooksu tüsistused. ASA pluss dipüridamooli rühma patsientidel vähenes risk 20% (p
PRoFESS (ennetusrežiim teise insuldi efektiivseks vältimiseks) on paralleelrühma randomiseeritud rahvusvaheline topeltpime kahekordne näiv, aktiivselt kontrollitud ja platseebokontrollitud uuring 2x2 teguriga, milles võrreldi AGGRENOXi klopidogreeliga ja telmisartaani platseeboga. insuldi ennetamiseks patsientidel, kellel oli varem esinenud mittekardioemboolse päritoluga isheemiline insult.
Kokku randomiseeriti 20 332 patsienti ravile AGGRENOXiga (n = 10 181) või klopidogreeliga (n = 10 151). Esmane tulemusnäitaja oli aeg enne insuldi esimest kordumist.
Esmase tulemusnäitaja esinemissagedus oli mõlemas ravirühmas sarnane (9,0% AGGRENOXi ja 8,8% klopidogreeli puhul; HR 1,01, 95% CI 0,92 - 1,11).Mitmete teiste oluliste eelnevalt määratletud tulemusnäitajate, sealhulgas korduva insuldi, müokardiinfarkti või veresoonkonna põhjustatud surma lõpp-tulemusnäitajate puhul ei leitud olulist erinevust AGGRENOXi ja klopidogreeli ravigruppide vahel (13,1% mõlemas ravigrupis; HR 0,99, 95%) CI 0,92 ... 1,07) ja korduva insuldi või suure verejooksu tulemusnäitaja (11,7% AGGRENOXi ja 11,4% klopidogreeli puhul; HR 1,03, 95% CI 0,95 - 1,11).
Neuroloogilist funktsionaalset tulemust 3 kuud pärast korduvat insuldi hinnati modifitseeritud Rankini skaalaga (mRS) ja mRS jaotuses ei täheldatud olulist erinevust AGGRENOXi ja klopidogreeli vahel (p = 0,3073 Cochran-Armitage'i testist lineaarse trendi järgi).
Eksperimentaalsed andmed näitavad, et ibuprofeen võib ravimite samaaegsel manustamisel pärssida atsetüülsalitsüülhappe väikeste annuste toimet trombotsüütide agregatsioonile. Ühes uuringus, pärast ibuprofeeni ühekordse 400 mg annuse manustamist 8 tunni jooksul enne või 30 minutit pärast atsetüülsalitsüülhappe (81 mg) manustamisel vähenes atsetüülsalitsüülhappe toime tromboksaani moodustumisele ja trombotsüütide agregatsioonile. Piiratud andmed ja ebakindlus seoses nende rakendamisega kliinilises olukorras ei võimalda siiski teha lõplikke järeldusi ibuprofeeni kasutamise jätkamise kohta; tundub, et ibuprofeeni aeg -ajalt kasutamisel puudub kliiniliselt oluline toime.
05.2 Farmakokineetilised omadused
Dipüridamooli toimeainet prolongeeritult vabastavate graanulite ja atsetüülsalitsüülhappe vahel puudub oluline koostoime. Seetõttu on AGGRENOXi farmakokineetika seotud nende kahe komponendi individuaalse farmakokineetikaga.
Dipüridamool
(Enamik andmeid viitab tervetele vabatahtlikele).
Annuse lineaarsust täheldati dipüridamooli kasutamisel kõigis ravis kasutatud annustes.
Pikaajaliseks raviks on välja töötatud modifitseeritud vabanemisega kapslid, mis sisaldavad graanulitena dipüridamooli. Dipüridamooli pH-st sõltuv lahustuvus, mis takistab lahustumist seedetrakti alumises osas (kus toimeainet prolongeeritult vabastavad preparaadid ei ole veel toimeainet vabastanud), on ületatud viinhappega; aeglustav efekt saavutatakse difusioonmembraaniga, mis pihustatakse graanulitele.
Mitmed püsiseisundi kineetilised uuringud näitavad, et kõik sobivad farmakokineetilised parameetrid, mis iseloomustavad toimeainet modifitseeritult vabastava preparaadi omadusi, on samaväärsed või mõnevõrra paranenud, kui toimeainet modifitseeritult vabastavaid dipüridamooli kapsleid manustatakse kaks korda päevas, võrreldes dipüridamooli kolme tabletiga neli korda päevas. Biosaadavus on veidi suurem, tippkontsentratsioonid on sarnased, allavoolu kontsentratsioonid on tunduvalt suuremad ja piigi / minimaalse kõikumine on väike.
Imendumine
Absoluutne biosaadavus on ligikaudu 70%. Kuna esmase läbimise efekt eemaldab ligikaudu 1/3 manustatud annusest, võib eeldada, et dipüridamooli imendumine on pärast AGGRENOXi manustamist peaaegu täielik.
Maksimaalne plasmakontsentratsioon saavutatakse ligikaudu 2-3 tundi pärast 400 mg AGGRENOX (200 mg kaks korda päevas) manustamist. Keskmine maksimaalne tasakaalukontsentratsioon on 1,98 mcg / ml (vahemik 1,01 - 3,99 mcg / ml) ja minimaalne kontsentratsioon on 0,53 mcg / ml (vahemik 0,18 - 1,01 mcg / ml).
Toit ei mõjuta dipüridamooli farmakokineetikat AGGRENOXis.
Levitamine
Tänu suurele lipofiilsusele, log P 3,92 (n-oktanool / 0,1 n, NaOH), dipüridamool on levinud paljudes organites. Loomadel jaotub dipüridamool eelistatavalt maksas, seejärel kopsudes, neerudes, põrnas ja südames.
Intravenoosse manustamise korral täheldatud kiire jaotumise faasi ei saa pärast suukaudset manustamist näha.
Keskosa (Vc) jaotusruumala on ligikaudu 5 l (sarnane plasma mahuga). Näiv jaotusruumala püsiseisundis on ligikaudu 100 l ja peegeldab jaotumist erinevatesse sektsioonidesse.
Ravim ei läbi olulisel määral hematoentsefaalbarjääri.
Dipüridamooli ülekanne platsenta kaudu on väga madal. Ühel naisel oli rinnapiimas tuvastatav ligikaudu seitsmeteistkümnendik plasmakontsentratsioonist.
Dipüridamooli seondumine valkudega on ligikaudu 97–99% ja toimub peamiselt koos alfa -1 -happelise glükoproteiini ja albumiiniga.
Biotransformatsioon
Dipüridamooli metabolism toimub maksas. Dipüridamool metaboliseerub peamiselt konjugatsiooni teel glükuroonhappega, moodustades peamiselt monoglükuroniidi ja ainult väheses koguses diglikuroniidi. Plasmas moodustab umbes 80% kogu kogusest algne ühend ja 20% kogukogusest monoglikuroniid .
Dipüridamooli glükuroniidide farmakodünaamiline aktiivsus on tunduvalt madalam kui dipüridamooli.
Elimineerimine
Domineeriv poolväärtusaeg pärast suukaudset manustamist on ligikaudu 40 minutit, samuti pärast intravenoosset manustamist.
Lähteühendi eritumine neerude kaudu on ebaoluline (väljaheited sapi kaudu, enterohepaatilise ringluse mõningad jäljed).
Kogu kliirens on ligikaudu 250 ml / min ja keskmine viibimisaeg on ligikaudu 11 tundi (tuleneb sisemisest keskmisest viibimisajast umbes 6,4 tundi ja keskmisest imendumisajast 4,6 tundi).
Nagu intravenoosse manustamise korral, täheldati pikenenud lõplikku poolväärtusaega ligikaudu 13 tundi.
Sellel eliminatsiooni lõppfaasil on suhteliselt väike tähtsus, kuna see moodustab väikese osa kogu AUC-st, mida tõendab asjaolu, et tasakaalukontsentratsioon saavutatakse kahe päeva jooksul, kui manustatakse kahe toimeainet modifitseeritult vabastava kapsli igapäevast annust.
Pärast korduvat manustamist ei kogunenud märkimisväärselt ravimeid.
Kineetika eakatel
Eakate (> 65 -aastased) plasmakontsentratsioonid (AUC järgi) olid pärast tablettidega ravimist ligikaudu 50% kõrgemad ja pärast AGGRENOX -ravi ligikaudu 30% kõrgemad kui noorematel (
Sarnast plasmakontsentratsiooni tõusu eakatel patsientidel täheldati ESPS-2 uuringus Persantini, toimeainet modifitseeritult vabastavate kapslite ja AGGRENOXi kohta.
Kineetika neerukahjustusega patsientidel
Kuna eritumine neerude kaudu on väga madal (5%), ei ole neerupuudulikkuse korral oodata farmakokineetika muutusi. ESPS-2 uuringus täheldati patsientidel, kelle kreatiniini kliirens oli vahemikus 15 ml / min kuni> 100 ml / min. ei muutu dipüridamooli ega selle metaboolse glükuroniidi farmakokineetika, kui andmeid korrigeeriti vanusevahede alusel.
Kineetika maksakahjustusega patsientidel
Maksapuudulikkusega patsientidel dipüridamooli plasmakontsentratsioon ei muutu, kuid glükuroniidid (farmakodünaamiliselt mitteaktiivsed) suurenevad. Soovitatav on dipüridamooli doseerida piiranguteta, kui puuduvad kliinilised tõendid maksapuudulikkuse kohta.
Atsetüülsalitsüülhape
Imendumine
Pärast suukaudset manustamist imendub atsetüülsalitsüülhape kiiresti ja täielikult maos ja soolestikus. Ligikaudu 30% atsetüülsalitsüülhappe annusest hüdrolüüsitakse eelnevalt süstemaatiliselt salitsüülhappeks.
Maksimaalne plasmakontsentratsioon pärast AGGRENOXis sisalduva 50 mg atsetüülsalitsüülhappe annuse manustamist (25 mg kaks korda ööpäevas) saavutatakse pärast 30 minuti möödumist igast annusest ja maksimaalne kontsentratsioon tasakaalukontsentratsioonis on ligikaudu 360 ng / ml. Atsetüülsalitsüülhappe puhul. Salitsüülhappe plasmakontsentratsioon saavutatakse 60-90 minuti pärast ja see on ligikaudu 1100 ng / ml.
Toit ei mõjuta oluliselt AGGRENOXis sisalduva atsetüülsalitsüülhappe farmakodünaamikat.
Levitamine
Atsetüülsalitsüülhape muundatakse kiiresti salitsülaadiks, kuid see on ravimi peamine vorm plasmas esimese 20 minuti jooksul pärast suukaudset manustamist.
Atsetüülsalitsüülhappe plasmakontsentratsioon väheneb kiiresti, poolväärtusaeg on umbes 15 minutit. Selle peamine metaboliit, salitsüülhape, seondub tugevalt plasmavalkudega ja seondumine sõltub kontsentratsioonist (mittelineaarne). Madala kontsentratsiooni korral (kesknärvisüsteem, rinnapiim ja loote kuded).
Biotransformatsioon
Atsetüülsalitsüülhape metaboliseerub mittespetsiifiliste esteraaside poolt kiiresti salitsüülhappeks.
Salitsüülhape metaboliseerub salitsüüluriinhappeks, salitsüülfenoolglükuroniidiks, atsüülsalitsüülglükuroniidiks ja vähemal määral gentisiinhappeks ja gentisuriinhappeks. Peamised metaboliidid salitsüüluriinhape ja salitsüülfenoolglükuroniid moodustuvad kergesti -Menentide kineetika; muud metaboolsed rajad on esmatasandi protsessid.
Elimineerimine
Atsetüülsalitsüülhappe eliminatsiooni poolväärtusaeg plasmas on 15-20 minutit; peamise metaboliidi, salitsüülhappe, eliminatsiooni poolväärtusaeg on väikestes annustes (nt 325 mg) 2–3 tundi, mis võib pikeneda kuni 30 tunnini suuremate annuste tõttu, kuna ainevahetus on mittelineaarne ja seondub plasmavalkudega.
Üle 90% atsetüülsalitsüülhappest eritub neerude kaudu metaboliitidena.
Muutumatul kujul eritunud salitsüülhappe osa uriinis suureneb annuse suurenedes ja üldise salitsülaadi renaalne kliirens suureneb ka uriini pH tõustes.
Kineetika neerukahjustusega patsientidel
Raske neerupuudulikkusega (glomerulaarfiltratsiooni kiirus alla 10 ml / min) patsientidel tuleb vältida atsetüülsalitsüülhappe manustamist.
On teatatud üldise plasmakontsentratsiooni ja seondumata salitsüülhappe fraktsiooni suurenemisest.
Kineetika maksakahjustusega patsientidel
Raske maksapuudulikkusega patsientidel tuleb vältida atsetüülsalitsüülhappe manustamist. On teatatud salitsüülhappe sidumata fraktsiooni suurenemisest.
05.3 Prekliinilised ohutusandmed
Ühekordse annuse toksilisuse uuringutes pärast dipüridamooli ja atsetüülsalitsüülhappe kombinatsiooni suukaudset manustamist seostati ägedat toksilisust närilistega mitme grammi kilogrammi kohta ja koertel 900 mg / kg.
See vastas segus sisalduvale atsetüülsalitsüülhappe kogusele. Dipüridamooli kogusel ei leitud mingit täiendavat või sünergistlikku toimet, olenemata tegelikust suhtest (dipüridamool: atsetüülsalitsüülhape = 1: 0,125 või 1: 4 kuni 1: 6). Südame -veresoonkonna puudulikkust peetakse surmapõhjuseks.
Korduva annuse toksilisuse uuringutes dipüridamooli: atsetüülsalitsüülhappe suhtega 1: 4 kuni 1: 5 kuni 6 kuud manustati rottidele ja koertele kuni 400 mg / kg. Rottid talusid neid annuseid ilma ilmsete joobetunnusteta.
On leitud, et annused 200 mg / kg ja rohkem on koertele mürgised, põhjustades seedetrakti muutusi, mis on põhjustatud 320 mg / kg atsetüülsalitsüülhappe osakaalust ning müokardi ja endokardi häireid ning neerupõletikku, mis on põhjustatud 40 mg / kg dipüridamooli osakaalust. . Võrreldavaid muutusi leiti ka üksikute komponentide puhul sarnaste annuste korral. Seetõttu võib öelda, et kombinatsioon ei andnud mingeid märke, mis viitaksid täiendavale või tugevnenud toksilisele toimele.
Teratogeensuse uuringud viidi läbi rottidel ja küülikutel annustes kuni emaslooma toksilisuseni dipüridamooli ja atsetüülsalitsüülhappe suhtega 1: 5,4. Paralleelselt maksimaalse annusega ravitud rühmaga raviti teist rühma ainult aspiriiniga vastavas annuses. Määrati kõrvalmõju emasloomale toksiliste annuste kasutamisel (405 mg / kg rottidel, 135 mg / kg küülikutel), suurem resorptsioonikiirus, ulatudes rottidel 100% -ni, ja järglaste kehamassi vähenemine. Väärarenguid täheldati ainult rühmades, keda raviti ainult atsetüülsalitsüülhappega, kuid mitte rühmades, mida raviti dipüridamooli / atsetüülsalitsüülhappega.
Fertiilsusuuringuid ja perinataalse perioodi uuringuid on läbi viidud ainult üksikute komponentidega. Viljakuse kahjustust ei leitud. Atsetüülsalitsüülhappe teadaoleva toime tõttu kaugelearenenud rasedusel soovitatakse ravi dipüridamooli ja atsetüülsalitsüülhappe kombinatsiooniga ainult siis, kui see on tõeline prioriteet.
Ravi selle kombinatsiooniga on eriti vastunäidustatud raseduse viimasel trimestril.Kuna mõlemad kombinatsioonikomponendid erituvad rinnapiima, ei ole imetamise ajal ravi hoolimata madalast piimakontsentratsioonist soovitatav.
Mutageensuse põhjalik sõeluuring in vitro ja in vivo uuringutes ei näidanud märke, mis viitaksid mutageensuse ohule.
Kantserogeenset toimet uuriti rottidel ja hiirtel maksimaalsetes annustes 450 mg / kg, mis vastab 75 mg / kg dipüridamoolile ja 375 mg / kg atsetüülsalitsüülhappele. Puudusid andmed kantserogeensuse kohta.
06.0 FARMATSEUTILINE TEAVE
06.1 Abiained
Viinhape, povidoon, metakrüülhappe-metüülmetakrülaadi kopolümeer (1: 2), talk, araabikummi, hüpromelloosftalaat, hüpromelloos, triatsetiin, dimetikoon 350, steariin / palmitiinhape, laktoosmonohüdraat, alumiiniumstearaat, kolloidne ränidioksiid, maisitärklis, tselluloos, sahharoos, E 171; kapsel (kõva): želatiin, E 171, E 172, puhastatud vesi.
06.2 Sobimatus
Sobimatus teiste ravimitega ei ole teada.
06.3 Kehtivusaeg
3 aastat.
06.4 Säilitamise eritingimused
Hoida temperatuuril kuni 30 ° C, hoida pudel niiskuse eest kaitstult suletuna.
06.5 Vahetu pakendi olemus ja pakendi sisu
Läbipaistmatu valge polüpropüleenpudel lastekindla polüetüleeni ja polüpropüleenist keeratava korgiga.
06.6 Kasutamis- ja käsitsemisjuhised
Ei mingeid erijuhiseid.
07.0 MÜÜGILOA HOIDJA
BOEHRINGER INGELHEIM ITALIA S.p.A.
Lorenzini kaudu, 8
20139 Milano
08.0 MÜÜGILOA NUMBER
50 kapslit A.I.C. n. 033181037
60 kapslit A.I.C. n. 033181049
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV
01.10.2001/01.10.2006
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV
14. juuli 2015